STRESZCZENIE
TŁO Nie istnieje ostateczne leczenie choroby koronawirusowej 2019 (COVID-19). Miód i Nigella sativa (HNS) mają ustalone właściwości przeciwwirusowe, przeciwbakteryjne, przeciwzapalne i immunomodulujące. Dlatego zbadaliśmy skuteczność HNS przeciwko COVID-19. szeroki
METODY Przeprowadziliśmy wieloośrodkowe, kontrolowane placebo, randomizowane badanie kliniczne w 4 ośrodkach w Pakistanie. Do badania włączono dorosłych z COVID-19, którzy wykazali umiarkowaną lub ciężką postać choroby, potwierdzono metodą RT-PCR. Wykluczono pacjentów z niewydolnością wielonarządową, wspomaganiem respiratorem i chorobami przewlekłymi (z wyjątkiem cukrzycy i nadciśnienia). Pacjenci zostali losowo przydzieleni w stosunku 1:1 do otrzymywania miodu (1 g/kg/dzień) i nasion Nigella sativa (80 mg/kg/dzień) lub placebo do 13 dni wraz ze standardową opieką. Wyniki obejmowały złagodzenie objawów, usunięcie wirusa i 30-dniową śmiertelność w populacji z zamiarem leczenia. To badanie zostało zarejestrowane na ClinicalTrials.gov, NCT04347382 .
WYNIKITrzystu trzynastu pacjentów – 210 umiarkowanych i 103 ciężkich – poddano randomizacji od 30 kwietnia do 29 lipca 2020 r. Spośród nich 107 przydzielono do HNS, a 103 do placebo w umiarkowanych przypadkach. W ciężkich przypadkach 50 otrzymało HNS, a 53 placebo. HNS spowodował ∼50% skrócenie czasu potrzebnego do złagodzenia objawów w porównaniu z placebo (umiarkowane (4 dni w porównaniu z 7), współczynnik ryzyka [HR]: 6,11; 95% przedział ufności [CI]: 4,23-8,84, p<0,0001 i ciężki (6 wobec 13 dni) HR: 4,04; 95% CI, 2,46-6,64, P<0,0001). HNS również usunął wirusa 4 dni wcześniej niż w grupie placebo w umiarkowanych (6 vs 10 dni, HR: 5,53; 95% CI: 3,76-8,14, P<0,0001) i ciężkich (8,5 vs 12 dni, HR: 4,32; 95% CI: 2,62-7,13, P<0,0001). HNS dalej prowadził do lepszego wyniku klinicznego w dniu 6 z wznowieniem normalnej aktywności u 63,6% w porównaniu z 10. 9% wśród umiarkowanych przypadków (OR: 0,07; 95% CI: 0,03-0,13, P<0,0001) i wypis ze szpitala 50% vs 2,8% w ciężkich przypadkach (OR: 0,03; 95% CI: 0,01-0,09, P<0,0001 ). W ciężkich przypadkach śmiertelność była czterokrotnie niższa w grupie z HNS niż w grupie placebo (4% vs 18,87%, OR: 0,18; 95% CI: 0,02-0,92, p=0,029). Nie zaobserwowano działań niepożądanych związanych z HNS.
WNIOSEK HNS znacząco złagodził objawy, klirens wirusa i śmiertelność u pacjentów z COVID-19. W związku z tym HNS stanowi niedrogą terapię bez recepty i może być stosowany samodzielnie lub w połączeniu z innymi metodami leczenia w celu uzyskania działania wzmacniającego przeciwko COVID-19.
FINANSOWANIE Finansowane przez Smile Welfare Organization, kompleks medyczny Shaikh Zayed i Services Institute of Medical Sciences.
TŁO
Pandemia choroby koronawirusowej 2019 (COVID-19) zainfekowała ponad czterdzieści milionów ludzi i spowodowała ponad milion zgonów na całym świecie. Wobec braku skutecznej szczepionki profilaktycznej istnieje pilna potrzeba znalezienia skutecznych metod leczenia pacjentów z COVID-19. Idealne leczenie powinno przynajmniej przyspieszać powrót do zdrowia objawów, zmniejszać przenoszenie wirusa w środowisku z wcześniejszym usunięciem wirusa u zakażonych pacjentów i zmniejszać śmiertelność. W tym kontekście pewną skuteczność wykazały terapie obejmujące hydroksychlorochinę/azytromycynę, lopinawir-rytonawir, remdesiwir, deksametazon, osocze rekonwalescencyjne i terapie przeciwciałami. 1 - 4Jednak wciąż jest wiele do zrobienia, zanim będziemy mieli skuteczny schemat leczenia COVID-19. W tym celu przeprowadziliśmy badanie kliniczne, w którym zbadaliśmy potencjalną skuteczność połączenia miodu i Nigella sativa (HNS) w leczeniu pacjentów z COVID-19.
Oba składniki HNS mają działanie przeciwwirusowe, przeciwbakteryjne, przeciwzapalne i immunomodulujące o udowodnionym profilu bezpieczeństwa. 5 - 8 Korzystny wpływ miodu na różne wirusy, w tym wirus różyczki, wirus opryszczki pospolitej, wirus zapalenia wątroby i wirus ospy wietrznej i półpaśca opisano wcześniej. 6 Co więcej, badania dokowania molekularnego in silico wykazały, że sześć związków flawonoidowych z miodu może hamować replikację ciężkiego zespołu ostrej niewydolności oddechowej koronawirusa 2 (SARS-CoV-2), wiążąc się z wirusową proteazą cysteinową podobną do 3-chymotrypsyny. 9 Miód ma również silne działanie przeciwbakteryjne przeciwko klinicznie ważnym bakteriom Gram-dodatnim (opornym na metycylinę staphylococcus aureus metycylinę) oraz bakterie Gram-ujemne ( Pseudomonas aeruginosa, Enterobacter spp i Klebsiella ). Dodatkowo miód wykazał synergizm z innymi antybiotykami, takimi jak oksacylina, tetracyklina, imipenem i meropenem. 6 Stosowanie miodu nie tylko poprawia proliferację limfocytów T i B, ale także ich aktywność fagocytarną. Dodatkowo hamuje ekspresję ważnych cytokin prozapalnych, takich jak interleukina (IL) 1 beta i IL-6. Aktywność przeciwwirusowa, w której pośredniczą limfocyty, okazała się mało skuteczna wobec COVID-19, zwłaszcza biorąc pod uwagę nadmierne uwalnianie mediatorów prozapalnych pomimo limfocytopenii. Dlatego postuluje się, że miód odgrywa kluczową rolę w walce z COVID-19. 10Jego stosowanie okazało się być bardziej korzystne w infekcjach górnych dróg oddechowych niż zwykła opieka, zwłaszcza w kontekście częstotliwości i nasilenia kaszlu. 11
Nigella sativa (NS), szeroko stosowana roślina lecznicza z rodziny Ranunculaceae, powszechnie znana jako czarnuszka /Kalonji, wykazuje działanie przeciwwirusowe przeciwko różnym wirusom, takim jak ludzki wirus niedoboru odporności i wirus zapalenia wątroby typu C. 12 Wykazano również, że zmniejsza replikację SARS-CoV in vitro w hodowlach komórkowych. 13Badania dokowania molekularnego wykazały, że niektóre jego składniki, takie jak nigeledina, α-hederyna i tymochinon, wykazują wysokie powinowactwo do kilku enzymów i białek SARS-CoV-2. W rzeczywistości wykazują one lepszy wynik kompleksu energetycznego niż chlorochina, hydroksychlorochina i favipiravir – leki, które wykazały pewną aktywność przeciw SARS-CoV-2. NS wykazał właściwości przeciwbakteryjne przeciwko wielu bakteriom, w tym wrażliwym i opornym na leki S. aureus, P. aeruginosa, Helicobacter pylori i Escherichia coli. Ponadto NS wykazał synergizm ze streptomycyną i gentamycyną. Demoduluje również wydzielanie szeregu mediatorów prozapalnych i poprawia stosunek limfocytów T pomocniczych (T4) i T8 supresorowych (T8) przy zwiększonej aktywności komórek NK. Wykazuje również potencjalne radykalne wymiatanie. 14 , 15
Ponieważ miód i Nigella sativa wykazują nakładające się profile farmakologiczne, uznaliśmy, że połączenie może być bardziej skuteczne w łagodzeniu nasilenia choroby, kontrolowaniu replikacji wirusa i leczeniu pacjentów z COVID-19. Kombinację z powodzeniem stosowano w różnych stanach chorobowych. 16 - 18 W tym miejscu donosimy, że leczenie HNS skutkuje wcześniejszą rekonwalescencją i usunięciem wirusa u pacjentów z COVID-19.
METODOLOGIA
PROJEKT BADANIA
Badanie było zainicjowanym przez badacza, wieloośrodkowym, randomizowanym badaniem kontrolowanym placebo z ramami wyższości przeprowadzonym w czterech placówkach opieki medycznej w Pakistanie (Shaikh Zayed Post-Graduate Medical Complex, Services Institute of Medical Sciences, Doctor's Lounge i Ali Clinic; wszystkie zlokalizowane w Lahore) . Badanie zostało zatwierdzone przez instytucjonalną komisję rewizyjną podyplomowego kompleksu medycznego i usług Instytutu Nauk Medycznych im. Shaikha Zayeda i nadzorowane przez niezależny komitet sterujący badaniem. Badanie zostało przeprowadzone zgodnie z zasadami Dobrej Praktyki Klinicznej Wytycznych Międzynarodowej Konferencji ds. Harmonizacji.
PACJENCI/UCZESTNICY
Podejrzewani pacjenci z COVID-19 wykazującymi pozytywny wynik SARS-CoV-2 w RT-PCR wymazów z nosogardzieli w certyfikowanych przez Międzynarodową Organizację Normalizacyjną (ISO) laboratoriach wyznaczonych w Pakistanie, zostali przebadani przy użyciu ilościowej RT-PCR w czasie rzeczywistym. Randomizowano dorosłych mężczyzn i kobiety niebędące w ciąży, które zgłosiły się do lekarza w ciągu 96 godzin od wystąpienia choroby. Kryteria wykluczenia obejmowały łagodne lub brak objawów klinicznych, niezdolność do wyrażenia pisemnej zgody, dysfunkcję wielonarządową, wspomaganie wentylacji lub PaO2/FIO 2poniżej 100, wstrząs septyczny, znana nadwrażliwość na HNS i choroby przewlekłe inne niż nadciśnienie i cukrzyca. Wykluczono również pacjentów z dodatnim wynikiem badania przesiewowego SARS-CoV-2 w listach planowych do jakiejkolwiek procedury. Od każdego uczestnika lub jego prawnego przedstawiciela uzyskano pisemną świadomą zgodę, jeśli był zbyt chory, aby wyrazić zgodę.
RANDOMIZACJA I MASKOWANIE
Kwalifikujących się pacjentów stratyfikowano w stosunku 1:1 w oparciu o nasilenie objawów klinicznych na dwie grupy: łagodne do umiarkowanych (kaszel, gorączka, ból gardła, przekrwienie błony śluzowej nosa, złe samopoczucie i/lub duszność) oraz ciężkie przypadki (gorączka). i/lub kaszel z zapaleniem płuc, ciężką dusznością, niewydolnością oddechową, przyspieszonym oddechem (>30 oddechów/min) lub niedotlenieniem (SpO 2<90% w stosunku do powietrza w pomieszczeniu) Ciężkość choroby została zdefiniowana zgodnie z wytycznymi dotyczącymi postępowania klinicznego dla COVID-19 opracowanymi przez Ministerstwo Narodowej Służby Zdrowia Pakistanu. W każdej z tych dwóch grup pacjenci zostali losowo przydzieleni (metodą loterii) do grupy terapeutycznej i kontrolnej. Stratyfikacji dokonano za pomocą oprogramowania SAS w wersji 9.4 dla grup wiekowych, płci, wyjściowego nasilenia objawów i chorób współistniejących, aby zapewnić zrównoważenie wielkości grup w obu ramionach. Przeprowadziliśmy ukrywanie przydziałów za pomocą interaktywnego systemu odpowiedzi głosowych/internetowych do czasu zakończenia randomizacji w systemie za pomocą komputera lub telefonu. Opiekunowie i oceniający wyniki zostali zaślepieni pomocą badaczy z ośrodka w zapewnieniu uczestnikom i zamaskowanym klinicystom placebo lub schematu terapeutycznego w celu oceny klinicznej, wyniki laboratoryjne i radiologiczne. Analitycy danych zostali zaślepieni, korzystając z analityków statystycznych z innych instytucji, które nie miały żadnego konfliktu interesów badawczych. Wszystkie dane były rejestrowane na papierowych formularzach akt sprawy, a następnie dwukrotnie wprowadzane do elektronicznej bazy danych i zatwierdzane przez personel procesowy.
PROCEDURA
Grupa HNS otrzymywała miód (1 g) plus kapsułkowany Nigella sativanasiona (80 mg) na kg masy ciała doustnie w 2-3 podzielonych dawkach dziennie przez okres do 13 dni, podczas gdy grupa kontrolna otrzymywała placebo (puste kapsułki). Oba produkty uzyskały certyfikat czystości wydany przez wydział botaniki Government College University w Lahore w Pakistanie. Ponadto każdy pacjent w badaniu otrzymał standardową terapię (SCT) zgodnie z zaleceniami lekarza prowadzącego oraz wytycznymi postępowania klinicznego dla COVID-19 ustanowionymi przez Ministerstwo Narodowej Służby Zdrowia Pakistanu. SCT składało się głównie z leków przeciwgorączkowych, antybiotyków, antykoagulantów, steroidów, dodatkowego tlenu i wentylacji mechanicznej. Uczestnicy badania byli oceniani pod kątem objawów klinicznych codziennie przez badacza na miejscu przez 13 dni. W trakcie badania, gdy pacjent wyzdrowiał i pozostawał bezobjawowy przez 48 godzin,Rysunek 1). Jeśli wynik testu był ujemny, uznawano, że wyleczył się z infekcji i leczenie zostało przerwane. W przypadku pozytywnego wyniku testu, trzeci test PCR przeprowadzono w dniu 14 bez dalszej obserwacji. Dla każdego pacjenta w dniu 0, 4, 6, 8, 10 i 12 odnotowywano ocenę kliniczną (CGS) dla każdego pacjenta. Opierała się ona na siedmiopunktowej skali porządkowej: stopień 1 (nie hospitalizowano, brak objawów zakażenia i wznowienie normalna aktywność), stopień 2 (nie hospitalizowany, ale niezdolny do wznowienia normalnej aktywności), stopień 3 (hospitalizowany, niewymagający dodatkowego tlenu), stopień 4 (hospitalizowany, wymagający dodatkowego tlenu), stopień 5 (hospitalizowany, wymagający tlenu o dużym przepływie przez nos terapia i/lub nieinwazyjna wentylacja mechaniczna), stopień 6 (hospitacja, wymagająca ECMO i/lub inwazyjnej wentylacji mechanicznej) i stopień 7 (zgon).2 Nasilenie objawów sklasyfikowano jako łagodną chorobę, w tym pacjentów z łagodnymi objawami COVID-19, ale bez radiologicznych dowodów zapalenia płuc. Choroba umiarkowana obejmowała pacjentów z niedotlenieniem (saturacja tlenem <94%, ale >90%) lub RTG klatki piersiowej z naciekami obejmującymi <50% pól płucnych lub gorączką, kaszlem, produkcją plwociny i innymi objawami ze strony układu oddechowego. Ciężką chorobę zdefiniowano jako obecność SaO 2 /SpO 2 poniżej 90% w powietrzu w pomieszczeniu lub PaO 2 do FiO 2współczynnik 300 lub niższy lub dowody radiologiczne wykazujące ponad 50% zajęcie płuc. Zmierzono temperaturę ciała, a gorączkę oceniono jako brak gorączki (98-99 °F), łagodną (>99-<100 °F), umiarkowaną (100-101,9 °F) i ciężką (≤102°F). Kaszel został sklasyfikowany jako łagodny (sporadyczny, ale przejściowy kaszel), umiarkowany (częsty, ale nieznacznie wpływający na czynności dzienne) i ciężki (częsty kaszel, ale znacząco wpływający na czynności dzienne). Skrócenie oddechu zostało sklasyfikowane jako Stopień 1 (bez zadyszka, z wyjątkiem forsownych ćwiczeń), stopień 2 (krótki oddech podczas spieszenia się na poziomie lub wchodzenie na niewielkie wzgórze), stopień 3 (chodzi wolniej niż większość ludzi na tym poziomie, zatrzymuje się po około mili lub zatrzymuje się po 15 minutach marszu we własnym tempie), stopień 4 (ubrania na oddech po przejściu około 100 jardów lub kilku minut po płaskim terenie) i stopień 5 (zbyt zadyszany, by wyjść z domu lub zadyszany podczas rozbierania się). Bóle mięśni i „jak bardzo czujesz się chory” były subiektywnymi odczuciami ocenianymi na 10-punktowej tabeli i klasyfikowanymi jako łagodne, umiarkowane i ciężkie. Poziomy białka C-reaktywnego w surowicy (CRP) mierzono za pomocą zestawu ELISA (Invitrogen, USA). Wyniki dotyczące bezpieczeństwa, w tym zdarzenia niepożądane, zostały skategoryzowane zgodnie z National Cancer Institute Common Terminology Criteria for Adverse Events, wersja 4.0. Badania laboratoryjne były oceniane jako część protokołu zgodnie z zaleceniami lekarza prowadzącego. Komitet sterujący badaniami monitorował bezpieczeństwo badań. W przypadku pacjentów, którzy zostali wypisani przed 13 dniem lub zostali poddani kwarantannie domowej, obserwację przeprowadzono za pomocą telemedycyny.
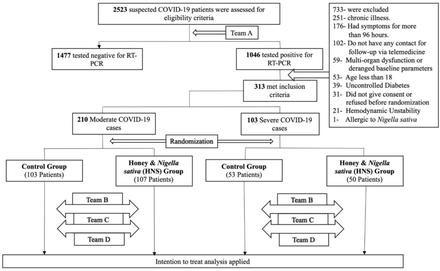
- Pobierz rysunek
- Otwórz w nowej karcie
Zespół A: Odpowiedzialny za rekrutację i testy SARS-CoV-2 RT-PCR; Zespół B: Codziennie oceniał stopień gorączki, kaszel, bóle mięśniowe, duszność, terapię tlenową, „jak bardzo się czujesz” i oceniaj stan emocjonalny; Zespół C: Zgłoszona skala oceny klinicznej (CGS) na siedmiopunktowej skali porządkowej oceny jako 0, 4, 6, 8, 10 i 12 dni; Zespół D przeprowadził kontrolne oznaczenia PCR i CRP.
WYNIKI
Pierwszorzędowymi punktami końcowymi były klirens wirusa (ujemny RT-PCR dla SARS-CoV-2 RNA), złagodzenie objawów klinicznych i obniżenie CGS w dniu 6. Drugorzędowe wyniki obejmowały zmniejszenie stopnia gorączki (dzień 4), poziomów CRP (dzień 6) , nasilenie objawów (8 dzień), wynik CGS (dzień 10) i śmiertelność w dniu 30. Dodatkowe wyniki obejmowały medianę czasu do klinicznej poprawy nasilenia objawów, stopień gorączki, kaszel, duszność, ból mięśni i czy czujesz". Mediana czasu do poprawy klinicznej została oceniona jako poprawa w jednej lub dwóch kategoriach lub osiągnięcie stanu normalnego w porządkowej skali wyników klinicznych.
ANALIZA STATYSTYCZNA
Wielkość próby nie została oszacowana w momencie planowania badania, ponieważ było to pierwsze tego typu badanie, a liczba włączonych pacjentów była uzależniona od obciążenia pacjentami w placówkach klinicznych, chociaż z góry określono 3-miesięczny okres. Skuteczność oceniano na podstawie analizy zamiaru leczenia losowo przydzielonych grup w przypadkach umiarkowanych i ciężkich. Niezależna komisja monitorująca dane co miesiąc przeglądała odkryte analizy danych z badania i wszelkie istotne informacje. W analizach jednoczynnikowych wykorzystaliśmy test log-rank do porównania czasu potrzebnego do usunięcia wirusa, złagodzenia objawów, czasu do poprawy nasilenia objawów klinicznych, stopnia gorączki, kaszlu, duszności, bólu mięśni i „jak bardzo jesteś chory”. czuć". Do oszacowania krzywych przeżycia dla czasu złagodzenia objawów i usunięcia wirusa zastosowano metodę Kaplana Meiera. Do porównania śmiertelności 30-dniowej zastosowano dokładny test Fishera. W analizach wielowymiarowych wykorzystaliśmy wielowymiarowe modele regresji, aby skorygować wpływ wieku (<40 lub >=40), płci, wyjściowego stopnia zaawansowania klinicznego, historii cukrzycy/nadciśnienia tętniczego i zużycia tlenu. W analizach wielowymiarowych wyników porządkowych wykorzystaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla wyników ciągłych, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov, Do porównania śmiertelności 30-dniowej zastosowano dokładny test Fishera. W analizach wielowymiarowych wykorzystaliśmy wielowymiarowe modele regresji, aby skorygować wpływ wieku (<40 lub >=40), płci, wyjściowego stopnia zaawansowania klinicznego, historii cukrzycy/nadciśnienia tętniczego i zużycia tlenu. W analizach wielowymiarowych wyników porządkowych wykorzystaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla ciągłego wyniku, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov, Do porównania śmiertelności 30-dniowej zastosowano dokładny test Fishera. W analizach wielowymiarowych wykorzystaliśmy wielowymiarowe modele regresji w celu dostosowania do wpływu wieku (<40 lub >=40), płci, wyjściowego stopnia zaawansowania klinicznego, historii cukrzycy/nadciśnienia tętniczego i zużycia tlenu. W analizach wielowymiarowych wyników porządkowych wykorzystaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla ciągłego wyniku, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov, zastosowaliśmy wieloczynnikowe modele regresji w celu dostosowania do wpływu wieku (<40 lub >=40), płci, wyjściowego stopnia klinicznego, cukrzycy/nadciśnienia w wywiadzie oraz zużycia tlenu. W analizach wielowymiarowych wyników porządkowych wykorzystaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla ciągłego wyniku, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov, zastosowaliśmy wieloczynnikowe modele regresji w celu dostosowania do wpływu wieku (<40 lub >=40), płci, wyjściowego stopnia klinicznego, cukrzycy/nadciśnienia w wywiadzie oraz zużycia tlenu. W analizach wielowymiarowych wyników porządkowych wykorzystaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla ciągłego wyniku, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov, zastosowaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla ciągłego wyniku, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov, zastosowaliśmy porządkowe modele regresji logistycznej zakładając proporcjonalne szanse. Wykorzystaliśmy również model regresji liniowej do analizy modeli proporcjonalnych hazardów CRP i Coxa dla ciągłego wyniku, aby przeanalizować czas do złagodzenia objawów i czas do usunięcia wirusa. Do tych analiz użyto oprogramowania SAS w wersji 9.4 (SAS Institute Inc., Cary, NC). To badanie jest zarejestrowane na ClinicalTrials.gov,NCT04347382 .
ROLA ŹRÓDŁA FINANSOWANIA
Badanie zostało sfinansowane przez szpitale i instytuty badawcze uczestniczące w badaniu HNS-COVID-PK. Organizacja Smile Welfare Organization (SWO) zapewniła dodatkowe finansowanie i wsparcie logistyczne dla badania. Ta organizacja non-profit przekazała również i dostarczyła badane leki i pulsoksymetry. Nie odgrywali jednak żadnej roli w prowadzeniu badania, projektowaniu badań, gromadzeniu danych, analizie danych, interpretacji danych ani pisaniu raportu. Proces nadzorował niezależny międzynarodowy komitet sterujący procesem. Komitet Wykonawczy ręczy za kompletność i dokładność danych oraz wierność badania z protokołem (patrz Dodatek Uzupełniający. Autor korespondencyjny miał pełny dostęp do wszystkich danych w badaniu i ponosił ostateczną odpowiedzialność za przedłożenie publikacji.
WYNIKI
Dwa tysiące pięćset dwudziestu trzech pacjentów z podejrzeniem COVID-19 zostało poddanych badaniom przesiewowym od 30 kwietnia do 29 lipca 2020 r., W których 1046 pacjentów uzyskało pozytywny wynik testu na obecność kwasu nukleinowego SARS-CoV-2. Spośród tych uczestników 313 spełniło kryteria włączenia ( Rysunek 1 ). Spektrum ich objawów klinicznych podzielono na dwie grupy: umiarkowaną i ciężką. Obie grupy liczyły odpowiednio 210 i 103 pacjentów. Pacjenci z każdej z dwóch grup zostali losowo przypisani do grupy leczonej i kontrolnej. Liczba pacjentów z umiarkowaną kontrolą, umiarkowanym HNS, ciężką kontrolą i ciężkim HNS wynosiła odpowiednio 103, 107, 53 i 50. Wyjściowe dane demograficzne z parametrami klinicznymi i laboratoryjnymi przedstawiono na: Tabeli 1. Paracetamol i azytromycyna były dwoma najczęściej przepisywanymi lekami w ramach SCT. Dwóch pacjentów zdecydowało się na kwarantannę domową pomimo konieczności terapii tlenowej.
- Zobacz wbudowane
- Wyświetl wyskakujące okienko
WYNIKI PIERWOTNE
Podstawowe wyniki przedstawiono w Tabeli 2 . Złagodzenie objawów COVID-19 u pacjentów w grupach HNS wystąpiło wcześniej niż w grupach kontrolnych: 4 w porównaniu z 7 dniami u pacjentów o umiarkowanym nasileniu (HR: 6,11; 95% CI: 4,23-8,84; P<0,0001) i 6 w porównaniu z 13 pacjenci z ciężką chorobą (HR: 4,04; 95% CI: 2,46-6,64; P<0,0001). Klirens wirusa (brak wyniku w teście SARS-CoV-2 RT-PCR) wystąpił 4 dni wcześniej w grupie z HNS zarówno w przypadku umiarkowanych (HR: 5,53; 95% CI: 3,76-8,14; P<0,0001) i ciężkich (HR : 4,32; 95% CI: 2,62-7,13; P<0,0001). Krzywe Kaplana-Meiera dla tych zmiennych pokazano na: rysunku 2. U pacjentów o umiarkowanym nasileniu w grupie z HNS wznowiono wcześniej, podczas gdy grupa kontrolna nie była w stanie wznowić codziennych czynności życiowych, o czym świadczy niższa mediana CGS w dniu 6 (iloraz szans: 0,07; 95% CI: 0,03-0,13; P<0,0001). Tymczasem w ciężkich grupach przypadki HNS zostały wypisane ze szpitala, podczas gdy przypadki kontrolne nadal hospitalizowano z dodatkowym tlenem zgodnie z medianą CGS w dniu 6 (iloraz szans: 0,03; 95% CI: 0,01-0,09; P<0,0001) .
- Zobacz wbudowane
- Wyświetl wyskakujące okienko
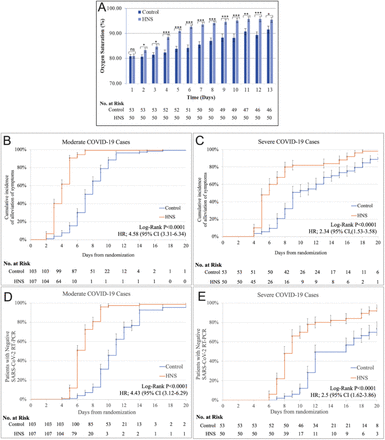
- Pobierz rysunek
- Otwórz w nowej karcie
A. Średnia saturacja tlenem spO2 w czasie w ciężkich przypadkach; krzywe prawdopodobieństwa Kaplana-Meiera dla czasu potrzebnego (w dniach) do złagodzenia objawów w przypadkach umiarkowanych (B) i ciężkich (C); Krzywe prawdopodobieństwa Kaplana-Meiera dla czasu potrzebnego (w dniach) do klirensu z fiolki w umiarkowanych (D) i ciężkich przypadkach (E).ns = nieistotne, *= P<0,05, **=P<0,001, ***= P<0,0001.
WYNIKI WTÓRNE
Wystąpiły istotne różnice we wszystkich drugorzędowych punktach końcowych między grupą leczoną i kontrolną (patrz Tabela 2dla wyników drugorzędnych). U pacjentów z umiarkowanym COVID-19 stopień gorączki (mediana) wynosił 100-101,9°F (umiarkowany) w grupie kontrolnej, podczas gdy uczestnicy ramienia HNS byli bezgorączkowi w dniu 4 (OR: 0,05; 95% CI: 0,03-0,1; P <0,0001). Istotną redukcję stopnia gorączki obserwowano w ciężkich przypadkach w 4. dobie (OR: 0,21; 95% CI: 0,09-0,46; P=0,0001). Poziomy CRP zmniejszyły się istotnie w dniu 6 w obu grupach z HNS w porównaniu z ich odpowiednimi grupami kontrolnymi (umiarkowane 6,15 ± 2,45 w porównaniu z 9,44 ± 4,94 mg/l, p <0,0001 i ciężkie przypadki 15,83 ± 7,17 w porównaniu z 23,32 ± 8,73 mg/l, p < 0,0001). W 8. dobie, zgodnie z medianą stopnia nasilenia objawów, 98,13% pacjentów było bezobjawowych w umiarkowanych przypadkach HNS w porównaniu do 56,31% w grupie kontrolnej (OR: 0,009; 95% CI: 0,001-0,08; P<0,0001). Podobnie w ciężkich przypadkach u większej liczby pacjentów w grupie HNS w ciężkich przypadkach występowały objawy bezobjawowe, podczas gdy większa liczba miała objawy umiarkowane (mediana) w ramieniu kontrolnym (OR: 0,1; 95% CI: 0,04-0,24). Do dnia 10. 96,26% przypadków umiarkowanych pacjentów w pełni wznowiło normalną aktywność z HNS w porównaniu z 68,93% w grupie kontrolnej (OR: 0,07; 95% CI: 0,02-0,21). W grupie ciężkiej mediana CGS w dniu 10. wykazała, że większość przypadków z grupy HNS powróciła do normalnej aktywności, podczas gdy pacjenci kontrolni nadal byli hospitalizowani i wymagali tlenoterapii (OR:0,05; 95% CI: 0,02-0,15). Rozkład pacjentów w kategoriach w skali porządkowej w czasie przedstawiono na: 26% pacjentów z umiarkowanymi przypadkami w pełni wznowiło normalną aktywność z HNS w porównaniu z 68,93% w grupie kontrolnej (OR: 0,07; 95% CI: 0,02-0,21). W grupie ciężkiej mediana CGS w dniu 10. wykazała, że większość przypadków z grupy HNS powróciła do normalnej aktywności, podczas gdy pacjenci kontrolni nadal byli hospitalizowani i wymagali tlenoterapii (OR:0,05; 95% CI: 0,02-0,15). Rozkład pacjentów w kategoriach w skali porządkowej w czasie przedstawiono na: 26% pacjentów z umiarkowanymi przypadkami w pełni wznowiło normalną aktywność z HNS w porównaniu z 68,93% w grupie kontrolnej (OR: 0,07; 95% CI: 0,02-0,21). W grupie ciężkiej mediana CGS w dniu 10. wykazała, że większość przypadków z grupy HNS powróciła do normalnej aktywności, podczas gdy pacjenci kontrolni nadal byli hospitalizowani i wymagali tlenoterapii (OR:0,05; 95% CI: 0,02-0,15). Rozkład pacjentów w kategoriach w skali porządkowej w czasie przedstawiono na:Rysunek 3 . Śmiertelność trzydziestodniowa wyniosła 18,87% w grupie kontrolnej i 4% z terapią HNS (OR: 0,18 95% CI: 0,02-0,92).
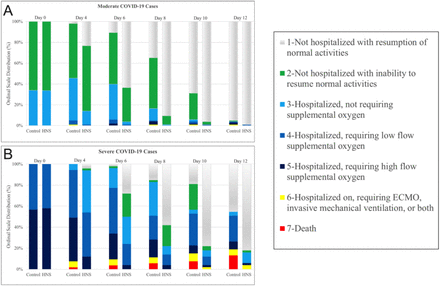
- Pobierz rysunek
- Otwórz w nowej karcie
Rysunek przedstawia zmiany kinetyczne w ocenie stopnia klinicznego (w 7-punktowej skali porządkowej) u pacjenta z COVID-19 otrzymującego leczenie (HNS) lub placebo (kontrola). Uwaga zwiększa liczbę pacjentów w skali 1 w grupie HNS zarówno w przypadkach umiarkowanych, jak i ciężkich.
DODATKOWE EFEKTY
W grupie HNS mediana osiągnięcia stanu normalnego w skali porządkowej była wcześniejsza pod względem nasilenia objawów (umiarkowane, 5 vs 8, HR; 4,49 (3,15-6,38), p<0,0001 i ciężkie, 7 vs 13 HR; 2,74 (1,68- 4,49), P<0,0001, stopień gorączki [4 wobec 8, HR; 4,17 (2,98-5,84), P<0,0001 i ciężki 6 wobec 10, HR; 2,64 (1,74-4,11), P<0,0001, stopień kaszlu [umiarkowany 5 wobec 7, HR; 2,67 (1,73-4,12), P<0,0001 i ciężki 6 wobec 9, HR; 2,04 (1,26-3,31), p=0,0001, stopień duszności (ciężkie 6 vs 13 HR; 2,39 (1,48-3,87), p<0,0001), nasilenie bólu mięśni (umiarkowane 4 vs 6 HR; 3,34 (2,14- 5,25, P<0,0001) ciężki 5 wobec 9, HR; 2,75 (1,62-4,69), p<0,0001 i „jak bardzo czujesz się chory” (umiarkowany 5 vs 8 HR (3,55 (2,55-4,93), p <0,0001 i ciężki 7 vs 13 HR; 2,87 (1,75-4,69), P<0,0001 ( Tabela 2). Podobne wyniki wcześniejszej poprawy klinicznej zaobserwowano w grupie HNS w odniesieniu do nasilenia objawów, stopnia gorączki, kaszlu, duszności, bólu mięśni i „jak się czujesz chory”. Ponadto w dodatkowych tabelach S2-S10 przedstawiono rozkład pod względem stopnia gorączki, kaszlu, bólu mięśni, uczucia nudności, stanu emocjonalnego, duszności, nasycenia tlenem, zapotrzebowania na tlen i nasilenia objawów w ciągu 13 dni. W przypadku HNS nie odnotowano wyraźnych działań niepożądanych.
DYSKUSJA
Badanie było wieloośrodkowym, randomizowanym, kontrolowanym placebo badaniem klinicznym badającym skuteczność terapeutyczną HNS przeciwko COVID-19. Zgodnie z naszą najlepszą wiedzą, ta próba jest pierwszym tego rodzaju, w którym badano kombinację dwóch naturalnych substancji. Obecne badanie wykazało lepszą skuteczność HNS w przypadku COVID-19 w większości badanych wyników. W grupach kontrolnych około połowa pacjentów wymagała 2-krotnie dłuższego czasu, aby stać się bezobjawowymi w porównaniu z grupami z HNS. Podobnie u >50% uczestników klirens wirusa nastąpił 4-5 dni wcześniej w grupach z HNS, co testowano metodą PCR. Średnie wysycenie tlenem powyżej 90%, w ciężkich przypadkach, osiągnięto 6 dni wcześniej przy leczeniu HNS ( ryc. 2). W grupie umiarkowanych przypadków do 4 dnia ponad połowa uczestników (grupa HNS) stała się bezgorączkowa, podczas gdy pacjenci z grupy kontrolnej utrzymywali się z umiarkowaną gorączką. Ponadto wśród ciężkich przypadków 22% (w porównaniu z 3,77%) pacjentów dotykało temperatury wyjściowej. Do 6 dnia, wśród umiarkowanych przypadków, większość pacjentów powróciła do normalnych codziennych czynności w grupie z HNS w porównaniu z ograniczoną aktywnością w grupie kontrolnej. Tymczasem wśród ciężkich przypadków większość pacjentów została wypisana do domu w grupach HNS, podczas gdy uczestnicy grupy kontrolnej nadal byli hospitalizowani, wymagając tlenoterapii. W 8. dniu, wśród przypadków umiarkowanych i ciężkich, odpowiednio 98,13% (w porównaniu z 56,31%) i 70% (w porównaniu z 19,61%) ustąpiło bezobjawowe po leczeniu HNS. Śmiertelność była około 4 razy wyższa w grupie kontrolnej. Wszystkie dane połączone, sugeruje silny profil terapeutyczny HNS, a wyniki mogą być bardzo zachęcające w obecnej drugiej fali zakażenia SARS-CoV-2. Ta doskonała skuteczność HNS jest przypisywana połączeniu kilku jego składników.
W przeciwieństwie do innych leków przeciwwirusowych, które celują w specyficzną strukturę lub szlak zakażenia SARS-CoV-2, HNS może zabijać/hamować wirusa poprzez strategię wielokierunkową poprzez celowanie w liczne miejsca wirusowe lub interakcje gospodarz-wirus. Na przykład, badania in-silico i in vitro przewidywały, że wiele flawonoidów i związków fenolowych obecnych w HNS, takich jak kaempferol, hesperydyna, chryzyna, kwercetyna i kwas linolowy jest przyłączonych/związanych z białkiem wypustkowym SARS-CoV-2 – ludzkim enzymem konwertującym angiotensynę kompleks receptora -2 (receptor do wiązania białek kolców nowego koronawirusa). 19 , 20Wśród flawonoidów w HNS szczególnie interesująca jest kwercetyna, która jest badana w wielu badaniach klinicznych przeciwko COVID-19. Poza przewidywanym wiązaniem kwercetyny do połączenia wirus-ludzkie białko, wiadomo również, że posiada właściwości przeciwbakteryjne poprzez rozrywanie błon, transport i ruchliwość. HNS zawiera również cynk, który ma ustalone właściwości przeciwwirusowe przeciwko kilku wirusom poprzez hamowanie replikacji wirusa i działanie jako środek immunomodulujący. 21Do tej pory trwa trzydzieści osiem badań klinicznych w celu sprawdzenia skuteczności cynku jako skutecznego środka przeciw COVID-19. Innym składnikiem HNS jest kwas askorbinowy (witamina C), powszechny przeciwutleniacz i wymiatacz wolnych rodników o właściwościach przeciwzapalnych, który redukuje mediatory takie jak IL-6 i endotelina-1. Ma również udowodnione właściwości przeciwdrobnoustrojowe i immunomodulujące oraz blokuje kilka kluczowych elementów burz cytokinowych. 22 , 23W tym celu zarejestrowano do tej pory czterdzieści pięć badań klinicznych z użyciem kwasu askorbinowego w celu sprawdzenia jego korzyści terapeutycznych jako profilaktyki i uzupełniającej terapii medycznej przeciwko COVID-19. W związku z tym HNS zawiera koktajl fitochemikaliów, które wzajemnie się uzupełniają, aby stawić czoła patologiom związanym z SARS-CoV-2. Na przykład kwercetyna jest jonoforem cynku i sugeruje się ich synergizm z witaminą C przeciwko SARS-CoV-2. 24 Wykazano również, że kwercetyna hamuje odpowiedzi cytokin prozapalnych (poprzez zmniejszenie prezentacji antygenu MHC klasy II i sygnalizacji TLR z aktywowanych komórek dendrytycznych), jednocześnie stymulując szlak T-helper 1 i szlak cytotoksyczny-CD8 do odpowiedniego usuwania wirusa. Co więcej, te procesy są dodatkowo wzmacniane przez obecność cynku, wzmacniając się nawzajem w skoordynowany sposób.19 W badaniu in vitro kwas linolowy (flawonoid) również wykazał synergię z lekiem COVID-19 remdesivirem, hamując replikację SARS-CoV-2. 20
Miód składa się głównie z cukrów z niewielką ilością aminokwasów, białek, enzymów, kwasów organicznych, witamin, minerałów, substancji lotnych i polifenoli. Właściwości antybakteryjne miodu przypisuje się wysokiemu stężeniu cukru, nadtlenku wodoru (H 2 O 2 ) i niskiemu pH wraz z metyloglioksalem i antybakteryjnym peptydem bee defensin-1. Obecność H 2 O 2 w miodzie nieodwracalnie uszkadza DNA drobnoustrojów poprzez generowanie rodników hydroksylowych. 5Ponadto miód wspomaga proliferację limfocytów, stymuluje fagocytozę i reguluje produkcję cytokin prozapalnych. Niektóre składniki (na przykład arabinogalaktany typu II, metyloglioksal i główne białko mleczka pszczelego-1) powodują działanie immunostymulujące lub prozapalne poprzez stymulowanie produkcji mediatorów immunologicznych, takich jak czynnik martwicy nowotworu α (TNF-α), IL-1β, i IL-6. Z drugiej strony, niektóre składniki (takie jak oksydaza glukozowa, kwas glukonowy, MGO i polifenole) wykazują działanie przeciwzapalne poprzez hamowanie produkcji niektórych cząsteczek, takich jak metaloproteinazy macierzy i reaktywne formy tlenu. 6
Aktywne składniki NS obejmują tymochinon (TQ), tymohydrochinon, ditymochinon, tymol, karwakrol, nigellicynę, nigellidynę i -hedrynę. Jednak jednym z integralnych składników nasion Nigella sativa jest TQ o hydrofobowości i stosunkowo mniejszych rozmiarach, które z łatwością przenikają przez błony plazmatyczne zakażonych komórek. Przechodząc do zakażonych komórek, TQ może wiązać się z lipofilową otoczką wirusa SARS-CoV-2 ze względu na swój hydrofobowy charakter, a tym samym niszczyć go przed wejściem do komórek. Wykazuje swój potencjał antybakteryjny zwłaszcza poprzez hamowanie syntezy biofilmu u niektórych bakterii. Wykazał swoje właściwości przeciwutleniające poprzez indukcję ekspresji i/lub aktywności transferazy S-glutationowej, peroksydazy glutationowej, dysmutazy ponadtlenkowej i reduktazy glutationowej. 7Moduluje lub hamuje odpowiedzi zapalne, np. IL-1, IL-6, IL-10, IL-18, TNF-α i czynnik jądrowy-κB, a zatem może znacznie zmniejszyć ryzyko śmiertelności związanej z burzą cytokinową COVID-19. 25
Przeciwcukrzycowe, przeciwnadciśnieniowe, kardioochronne i rozszerzające oskrzela właściwości HNS mogą uczynić go jeszcze bardziej korzystnym u pacjentów z cukrzycą, nadciśnieniem, sercem i astmą, którzy mają wyższą śmiertelność związaną z COVID-19. 12 , 26 Ponadto działanie przeciwpłytkowe i przeciwzakrzepowe HNS może również chronić pacjentów z COVID-19 przed powikłaniami zakrzepowo-zatorowymi, które należą do głównych powikłań i przyczyn śmiertelności. 27 Chroniący wątrobę i nerki charakter HNS może dawać dodatkowe pierwszeństwo przed innymi lekami w ograniczaniu uszkodzeń wątroby i nerek związanych z COVID-19. 12 , 26 Właściwości przeciwgorączkowe, przeciwbólowe i przeciwkaszlowe HNS mogą również łagodzić objawy. 11Co więcej, właściwości przeciwdrobnoustrojowe HNS i synergizm z innymi antybiotykami przeciwko nakładającym się infekcjom mogą zapobiegać zgonom związanym z sepsą. 6 , 8 , 14 Wytyczne NICE i Public Heath England zalecają również miód jako pierwszą linię leczenia ostrego kaszlu spowodowanego infekcjami górnych dróg oddechowych, znanego jako jeden z objawów definiujących COVID-19. Odkrycia te wzmacniają wykorzystanie HNS jako potencjalnego kandydata do zwalczania SARS-CoV-2 na całym świecie.
W porównaniu z tym, czas powrotu do zdrowia zgłaszany dla remdesiwiru wynosił 10 dni w porównaniu z 15 dniami dla kontroli (P<0,001), 3 podczas gdy lopinawir-rytonawir nie powodował skrócenia czasu powrotu do zdrowia (16 dni w porównaniu z 16 dniami; P=0,09) . 2 W naszym badaniu w około 50% przypadków SARS-CoV-2 RT-PCR w grupach z HNS wykazywał ujemny wynik 4 dni wcześniej niż w grupach kontrolnych. We wcześniejszych badaniach śmiertelność wśród ciężkich przypadków w porównaniu z grupą kontrolną wynosiła 27,0% (w porównaniu z 25,0%) dla hydroksychlorochiny, 1 19,2% (w porównaniu z 25,0%) dla lopinawiru-rytonawiru, 2 15,7% (w porównaniu z 24,0%) dla osocza rekonwalescencyjnego, 28 11,4% (w porównaniu z 15,2%) dla remdesiwiru, 3 22,9% (w porównaniu z 25,7%) dla deksametazonu, 4i tylko 4% (w porównaniu z 18,87%) dla HNS. W ten sposób HNS zapewnił przewagę kliniczną w zmniejszaniu śmiertelności u pacjentów z COVID-19. Warto zauważyć, że połączone dane dotyczące śmiertelności dostarczone przez Solidarity i ACTT-1 dla remdesiwiru oraz przez badanie Solidarity and Recovery dla lopinawiru-rytonawiru nie zapewniły statystycznej poprawy śmiertelności. 29 W przeciwieństwie do tych leków, HNS stanowi bezpieczniejszą i tańszą opcję, którą można stosować jako lek wewnętrzny.
Głównym ograniczeniem tego badania było to, że miód i NS nie były podawane pacjentom jako leczenie oddzielnie. Do tego badania nie włączono pacjentów korzystających ze wspomagania respiratora. Aby zbadać potencjalne różnice w odpowiedzi na leczenie u pacjentów z COVID-19 o różnym pochodzeniu rasowym i etnicznym, wymagane jest międzynarodowe badanie na większej próbie.
WNIOSEK
Podsumowując, HNS okazał się bezpiecznym i skutecznym lekarstwem dla pacjentów z COVID-19. Promuje usuwanie wirusa, szybszy powrót do zdrowia i zmniejsza śmiertelność. Jego przystępność cenowa (<5 USD za cały cykl leczenia), dostępność bez recepty i łatwość podawania (jako łatwy lek do domu) sprawiają, że leczenie to jest jeszcze bardziej wykonalne. Ponadto, jako niedrogi nutraceutyk, HNS może być stosowany samodzielnie lub w połączeniu z innymi lekami w celu uzyskania efektu addytywnego. Jest bardzo prawdopodobne, że leczenie w znaczący sposób zmniejszy obciążenie systemów opieki zdrowotnej.
Badania w kontekście
Dowody przed tym badaniem
Przeszukaliśmy PubMed od momentu powstania do 29 kwietnia 2020 r. pod kątem badań klinicznych opublikowanych w języku angielskim sprawdzających potwierdzoną skuteczność dowolnego leku przeciwko COVID-19 przy użyciu wyszukiwanych haseł („COVID-19” [Wszystkie pola] LUB „SARS-CoV-2” [Wszystkie pola]) (filtry: badanie kliniczne, randomizowane badanie kontrolowane). W randomizowanych badaniach klinicznych nie zidentyfikowaliśmy żadnego leku o udowodnionej skuteczności przeciwko COVID-19. W międzyczasie przeszukaliśmy również PubMed pod kątem leków, które mogą być dostępne na całym świecie i są skuteczne przeciwko wirusom i innym drobnoustrojom, a także mają właściwości przeciwzapalne, immunomodulujące i antykoagulacyjne o szerokim profilu bezpieczeństwa. Wszystkie artykuły oryginalne, publikacje przeglądowe,Stwierdzono, że do poszukiwań najbardziej nadaje się Nigella sativa . Nie zidentyfikowano żadnego opublikowanego badania klinicznego dotyczącego wpływu miodu i Nigella sativa na pacjentów z COVID-19.
Wartość dodana tego badania
Zgodnie z naszą najlepszą wiedzą, to badanie jest pierwszym randomizowanym, kontrolowanym placebo badaniem klinicznym oceniającym skuteczność doustnego miodu i nasion Nigella sativa wśród dorosłych z umiarkowanym lub ciężkim COVID-19. W analizie zgodnej z zaplanowanym leczeniem przedstawiliśmy wyczerpujące metodyczne opisy parametrów klinicznych i wyników klinicznych. U pacjentów z COVID-19 miód i Nigella sativa ze standardową terapią opiekuńczą spowodowały wcześniejsze usunięcie wirusa, złagodzenie objawów, poprawę kliniczną i zmniejszenie śmiertelności. Ponadto, podobnie jak w poprzednich badaniach, nie zgłoszono żadnych działań niepożądanych dotyczących HNS.
Implikacje wszystkich dostępnych dowodów
Biorąc pod uwagę kryzys gospodarczy związany z pandemią COVID-19, stosowanie miodu i Nigella sativa będzie szczególnie korzystne dla zubożałych populacji w środowiskach o ograniczonych zasobach. Niedrogi schemat leczenia bez recepty byłby cennym źródłem zmniejszenia obciążenia systemu opieki zdrowotnej, a jednocześnie znacznie osłabiłby wpływ choroby. Dodanie tych dwóch nutraceutyków przyniesie wielką wartość w celu obniżenia zachorowalności/śmiertelności w przypadku COVID-19. Badanie wpłynie na praktykę kliniczną i bezpośrednie przyszłe badania w dziedzinie pojawiających się chorób zakaźnych. Niemniej jednak odkrycia te powinny zostać przetestowane i powtórzone w dalszych międzynarodowych, większych badaniach klinicznych.
Dostępność danych
Dane kliniczne są dostępne jako dodatkowy plik, a surowe dane mogą być dostarczone na żądanie do odpowiedniego autora
WKŁAD AUTORÓW
SA i ShA w równym stopniu przyczynili się do powstania tego artykułu i współdzielą współautorstwo. TM, QAS, AA, MA i MI są starszymi autorami. MA, MAI, LK, UNS i IF były współgłównymi autorami tego szkicu. SA, MAI, AA i MA wnieśli wkład w koncepcję, projektowanie, pozyskiwanie danych, redagowanie rękopisów i wkład intelektualny. SA i MON zaproponowały hipotezę i projekt badania oraz uzyskały dofinansowanie. RA, MSS, KH, HR i ABA dodały wyniki badań do ośrodków badawczych. MA, MoA, SiA i MFN wniosły wkład biochemiczny, farmakologiczny i farmaceutyczny wraz z dozymetrią. MKA, SoA, MAz i HZ kierowały rozwojem czyszczenia i analizy danych oraz wzięły odpowiedzialność za wyniki w tym projekcie i przyszłej analizie. SA, MoA, RA i AH opracowały pierwszą wersję rękopisu. NM, IF, SR, AbH, ZA, AK, ZH, ShaA, HR, ABA, KH i AAr reprezentowali prowadzenie i walidację kompilacji i analizy danych w manuskrypcie. KN, MSu, SZ, IA, AH, AM, TM, SS, MeA, AA, MA, QAS i MI przeoczyły prowadzenie i ważność badania, a także przyczyniły się do wkładu intelektualnego w protokół badania i metodologię wraz z ostatecznym napisaniem manuskryptu w górę. MeA i MI zapewniły w swoich instytutach zasadność gromadzenia i analizy danych oraz rozważania etyczne. Wszyscy autorzy są odpowiedzialni za swój wkład, zapewniając krytyczne redakcje i ostateczną autoryzację artykułu. Autor korespondencyjny potwierdza autentyczność, że wszyscy wymienieni autorzy spełniają kryteria autorstwa. QAS i MI przeoczyły przebieg i ważność badania, a także wniosły wkład intelektualny w protokół badania i metodologię wraz z końcowym zapisem manuskryptu. MeA i MI zapewniły w swoich instytutach zasadność gromadzenia i analizy danych oraz rozważania etyczne. Wszyscy autorzy są odpowiedzialni za swój wkład, dostarczając krytyczne redakcje i ostateczną autoryzację artykułu. Autor korespondencyjny potwierdza autentyczność, że wszyscy wymienieni autorzy spełniają kryteria autorstwa. QAS i MI przeoczyły przebieg i ważność badania, a także wniosły wkład intelektualny w protokół badania i metodologię wraz z końcowym zapisem manuskryptu. MeA i MI zapewniły w swoich instytutach zasadność gromadzenia i analizy danych oraz rozważania etyczne. Wszyscy autorzy są odpowiedzialni za swój wkład, zapewniając krytyczne redakcje i ostateczną autoryzację artykułu. Autor korespondencyjny potwierdza autentyczność, że wszyscy wymienieni autorzy spełniają kryteria autorstwa. dostarczenie krytycznych edycji i ostatecznej autoryzacji artykułu. Autor korespondencyjny potwierdza autentyczność, że wszyscy wymienieni autorzy spełniają kryteria autorstwa. zapewnienie krytycznych edycji i ostatecznej autoryzacji artykułu. Autor korespondencyjny potwierdza autentyczność, że wszyscy wymienieni autorzy spełniają kryteria autorstwa.
PODZIĘKOWANIE
Autorzy pragną podziękować wszystkim członkom komitetu sterującego badaniem oraz pacjentom, którzy wzięli udział w tym badaniu. Specjalne podziękowania dla rządu Pakistanu i organizacji Smile Welfare za udostępnienie bezpłatnych obiektów do testowania COVID-19 oraz miodu i nasion Nigella sativa . Warto docenić wszystkich klinicystów, personel paramedyczny i laboratoryjny, którzy pomogli w przeprowadzeniu tego badania. Zespół chciałby podziękować prof. dr Zaheerowi Ahmadowi (profesor botaniki, Government University Lahore, Pakistan) za przetestowanie czystości miodu i Nigella sativa użytych w badaniu.
Przypisy
-
↵ 2 Wspólny pierwszy autor
-
↵ 3 wspólny drugi autor
-
zmiany w zapisie wg BMJ
BIBLIOGRAFIA
- 1. ↵
Google Scholar
- 2. ↵
Google Scholar
- 3. ↵
Google Scholar
- 4. ↵
Google Scholar
- 5. ↵
CrossRefPubMedSieć naukiGoogle Scholar
- 6. ↵
Google Scholar
- 7. ↵
Google Scholar
- 8. ↵
Google Scholar
- 9. ↵
Google Scholar
- 10. ↵
Google Scholar
- 11. ↵
Google Scholar
- 12. ↵
Google Scholar
- 13. ↵
Google Scholar
- 14. ↵
Google Scholar
- 15. ↵
Google Scholar
- 16. ↵
Google Scholar
- 17.
Google Scholar
- 18. ↵
Google Scholar
- 19. ↵
Google Scholar
- 20. ↵
Streszczenie / BEZPŁATNY pełny tekstGoogle Scholar
- 21. ↵
CrossRefGoogle Scholar
- 22. ↵
Google Scholar
- 23. ↵
Streszczenie / BEZPŁATNY pełny tekstGoogle Scholar
- 24. ↵
Google Scholar
- 25. ↵
Google Scholar
- 26. ↵
Google Scholar
- 27. ↵
Google Scholar
- 28. ↵
CrossRefPubMedGoogle Scholar
- 29. ↵
Google Scholar






