Raporty naukowe Tom 8 , Numer artykułu: 8764 ( 2018 )
Abstrakcyjny
W sumiczek szklisty (szkło szklisty) jest znanych z reagowania na działanie pola elektromagnetycznego (PEM). Tutaj przetestowaliśmy jego zachowanie unikające w odpowiedzi na stymulację statycznymi i zmiennymi polami magnetycznymi. Stosując klonowanie ekspresyjne zidentyfikowaliśmy elektromagnetyczny gen percepcyjny ( EPG ) z K. bicirrhiskodujący białko, które odpowiada na EMF. Ten gen EPG został sklonowany i wyrażony w komórkach ssaków, kulturach neuronalnych iw mózgu szczura. Badania immunohistochemiczne wykazały, że ekspresja EPG jest ograniczona do błony komórkowej ssaków. Obrazowanie wapnia w komórkach ssaków i hodowanych neuronach wyrażających EPG wykazało, że zdalna aktywacja przez EMF znacząco zwiększa wewnątrzkomórkowe stężenie wapnia, co wskazuje na pobudliwość komórkową. Co więcej, bezprzewodowa aktywacja magnetyczna EPG w korze ruchowej szczura indukowała reakcje wywołane ruchowo przeciwnej kończyny przedniej in vivo . W tym miejscu informujemy o rozwoju nowej technologii do zdalnej, nieinwazyjnej modulacji funkcji komórek.
Wprowadzenie
Większość dostępnych technologii do manipulowania funkcjami komórkowymi w sposób specyficzny dla komórki i czasoprzestrzeni wymaga użycia optyki 1 , 2 , 3 , 4 , 5 , 6 , 7 , leków 8 , 9 , 10 , ogrzewania falami radiowymi 11 , 12 , 13 lub ultradźwięków 14 . Jednak poszukiwanie genów kontrolujących funkcję komórek za pomocą pól elektromagnetycznych (EMF), które nieinwazyjnie wnikają w głęboką tkankę, jest dopiero w powijakach 15 , 16. Chociaż wiadomo, że różne gatunki wodne wykorzystują pola magnetyczne i elektryczne Ziemi do orientacji, nawigacji i wykrywania ofiar i drapieżników 17 , mechanizmy komórkowe tego samego pozostają nieznane. Jeden z takich organizmów, Kryptopterus bicirrhis , ryba słodkowodna, zawiera narząd bańkowy przeznaczony do wyczuwania pola elektromagnetycznego 17 . Dowody sugerują, że indukcja pola elektromagnetycznego powoduje natychmiastowy napływ wapnia do komórek elektroreceptorów narządów brodawkowych 18, które znajdują się pod płetwami. Tak więc jest prawdopodobne, że te komórki elektroreceptorowe wyrażają białka wrażliwe na zmiany w EMF. Zasadniczo identyfikacja białka, które jest zdalnie aktywowane przez nieinwazyjne pola elektromagnetyczne, jest niezaspokojoną potrzebą, która może uzupełnić rosnący arsenał technologii przeznaczonych do zewnętrznej kontroli aktywności komórkowej in vivo .
Wyniki
K. bicirrhis odpływa w odpowiedzi na pole elektromagnetyczne
Przetestowaliśmy reakcję behawioralną ryb na statyczne i zmienne pola magnetyczne. Czternaście K. bicirrhis umieszczono w 30-galonowym zbiorniku utrzymywanym w temperaturze 25°C (Fig. 1 ). Do testów behawioralnych ryby pogrupowano i umieszczono w zbiorniku. Neodymowy magnes ziem rzadkich umieszczono z jednej strony na 10 s, a ryby oddalone o 10 mm poddano działaniu pola o natężeniu 23 mT. Pozorny bodziec składał się z plastikowego przedmiotu podobnej wielkości. W tych próbach (n = 10) ryby przepłynęły odległość 344 ± 26 mm w odpowiedzi na bodziec magnetyczny, który był znacznie większy niż odległość 91 ± 5 mm (p < 10 -6 , test t Studenta). w pozorowanych eksperymentach (ryc. 1D). Do zmiennego pola magnetycznego zastosowano system przezczaszkowej stymulacji magnetycznej (TMS) przy 250 mT. W próbach pozorowanych cewka TMS została umieszczona z boku zbiornika i dostarczono tylko nagranie dźwiękowe. Podczas pozorowanych prób ryby były obojętne na dźwięk wydawany przez system TMS; na TMS w próbach eksperymentalnych, wszystkie ryby odpłynęły od źródła pola elektromagnetycznego. Rysunek 1A-C (oraz filmy S1 w danych uzupełniających) pokazuje pozycję ryb przed stymulacją EMF i ich pozycję w zbiorniku 1 s po wywołaniu EMF. Wyniki te pokazują, że ryby te wykazują silną reakcję behawioralną indukowaną przez statyczne i zmienne bodźce magnetyczne.
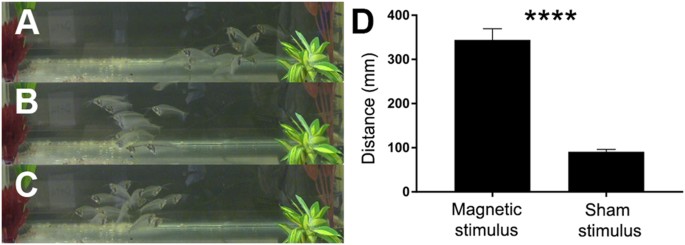
W K. bicirrhis odpłynąć w odpowiedzi na pola elektromagnetyczne. Cewka TMS została umieszczona po prawej stronie akwarium i indukowała impulsy o częstotliwości 50 Hz przez 5 sekund. ( A) Przed zastosowaniem stymulacji ryby były rozproszone w zbiorniku. ( B ) Podczas stymulacji wszystkie ryby odpłynęły od źródła stymulacji, które znajdowało się po prawej stronie. ( C ) Kiedy stymulacja się skończyła, ryba znów zaczęła pływać we wszystkich kierunkach. Ryby zostały nagrodzone pod koniec próby. ( D ) Statyczna stymulacja magnetyczna indukowała zachowanie unikające (****p < 10-6 ).
Klonowanie genu percepcji elektromagnetycznej
Aby zidentyfikować i scharakteryzować przypuszczalne białko(a) wrażliwe na EMF, zastosowaliśmy klonowanie ekspresyjne w oocytach 19 , 20 Xenopus laevis (X. laevis) . Wyizolowaliśmy chirurgicznie płetwę odbytową zawierającą narządy elektroreceptorowe 21 z 80 znieczulonych K. bicirrhis i wyekstrahowaliśmy całkowity mRNA, z którego skonstruowano bibliotekę cDNA. Podbiblioteki cDNA przeszukiwano za pomocą dwuelektrodowego zacisku napięciowego (TEVC) w oocytach X. laevis 22 , 23dla zmienionych odpowiedzi prądowych na stymulację. Jedna z podbibliotek wykazywała zwiększony, zależny od napięcia prąd błonowy w roztworach fizjologicznych (ND96) i bezsodowych (NMDG). W związku z tym 44 klony cDNA z tej podbiblioteki zamplifikowano i oczyszczono do dalszych badań przesiewowych. Klony zsekwencjonowano i wszystkie przypuszczalne geny porównano z bazą danych GenBank. Kandydujące otwarte ramki odczytu każdego przypuszczalnego genu poddano translacji i porównano z bazą danych białek. Klony podzielono dalej na mniejsze podbiblioteki, a aktualną odpowiedź zbadano za pomocą TEVC. Doprowadziło to do identyfikacji pojedynczej otwartej ramki odczytu kodującej białko o 133 aminokwasach (~15 kDa), które wykazywało konstytutywnie zwiększony prąd prostowania na zewnątrz, który nazwaliśmy genem percepcji elektromagnetycznej (EPG).
Stosując reakcję łańcuchową polimerazy z odwrotną transkrypcją (RT-PCR) ze specyficznymi starterami sprawdziliśmy, że EPG jest rzeczywiście konstytutywnie transkrybowane przez K. bicirrhis . (rysunek uzupełniający S1 ). Aby potwierdzić, że EPG ulega translacji (tj. tworzeniu białka), wytworzyliśmy poliklonalny oczyszczony przez powinowactwo przeciwko domniemanej domenie zewnątrzkomórkowej w oparciu o Genscript OptimumAntigen TM Design Program. Jak widać na ryc. uzupełniającym. S1 , linie 1–3, EPG jest wykrywane tylko w ekstrakcie tkankowym K. bicirrhis, ale nie w tkance kontrolnej z Danio Rerio ( Danio pręgowany), co wyraźnie wskazuje, że EPG jest unikalnym białkiem dla K. bicirrhis, który został wyewoluowany do pełnienia specyficznej funkcji . Warto zauważyć, że na podstawie masy cząsteczkowej EPG wydaje się być (homo)dimerem.
Analiza bioinformatyczna sekwencji DNA i białek EPG
Analiza BLASTN 24 sekwencji cDNA EPG nie dała żadnych dopasowań (unikalna identyczność) w nienadmiarowej bazie danych genomowego DNA. Analiza TBLASTX sekwencji cDNA, przy użyciu bazy danych znaczników sekwencji wyrażanych (dbEST) dała statystycznie istotne dopasowania z EST dla kilku ryb. Z sześciu możliwych otwartych ramek odczytu (ORF) EMBOSS ( 25 ), pierwszy ORF w wyniku pojedynczego białka, zgodnie ze zakodowanej sekwencji białkowej z poszukiwań TBLASTX. Poszukiwanie sekwencji aminokwasów metodą DELTA-BLAST dało zgodność z licznymi białkami z rodziny UPAR_LY6 (dostęp: pfam00021 ). Skonstruowaliśmy drzewo filogenetyczne białka EPG i jego homologów (metoda największego prawdopodobieństwa, model oparty na macierzy JTT 26), który pokazał ewolucyjny związek EPG z innymi białkami w tej samej nadrodzinie (rysunek uzupełniający S2 ). Wielokrotne dopasowanie sekwencji przy użyciu MUSCLE 27 , 28 (rysunek uzupełniający S3 ) wykazało, że EPG ma konserwatywną domenę bogatą w cysteinę. Domena ta jest homologiczna do domeny UPAR_LY6 (rysunek uzupełniający S3A , reszty aminokwasowe wytłuszczone na niebiesko).
Przewidywana struktura drugorzędowa EPG obejmuje pięć nici beta flankowanych przez helisy alfa na każdym końcu (JPred 29 , (rysunek uzupełniający. S3 ). Dalej modelowaliśmy orientację błonową EPG przy użyciu Polyphobius 30 , który wykazał hydrofobowy ( przezbłonowy ) N -końcowy peptyd sygnałowy (TMHMM 31 , Signal-Blast 32 ), po którym następuje region niecytoplazmatyczny (rysunek uzupełniający S3). Przypuszczalny region zewnątrzkomórkowy obejmuje pięć nici beta zlokalizowanych w domenie UPAR_LY6 białka EPG. Oparte na homologii modelowanie struktury trzeciorzędowej domniemanej zewnątrzkomórkowej domeny EPG (reszty 17–104) przewidziało wzbogaconą w arkusz beta domenę podobną do dysku z konserwowanymi cysteinami (SWISS-MODEL 33 , 34 , 35 , 36 , cysteiny pokazane jako sfery błękitne w (dodatkowy rys. S3 ). Wykres dostępności EPG ( dodatkowy rys. S3 )wygenerowany przy użyciu DeepView pokazuje wklęsły charakter domeny zewnątrzkomórkowej, podobny do domeny UPAR_Ly6 CD59. Wklęsła powierzchnia domeny UPAR_LY6 CD59 jest jej aktywną zewnątrzkomórkową domeną wiążącą 37 , 38 i wykazuje podobieństwo topologiczne do rodziny Toxin_1 39 , 40 . Stawiamy hipotezę, że wewnątrzcząsteczkowe wiązania dwusiarczkowe między konserwowanymi cysteinami EPG mogą pomóc ustabilizować jego domenę niecytoplazmatyczną (podobną do tych występujących w CD59). Domena niecytoplazmatyczna EPG zawiera również przewidywane miejsce N-glikozylacji w reszcie-77, co sugeruje, że EPG może być białkiem glikozylowanym.
Ekspresja EPG w komórce i regionie
Ludzkie komórki embrionalne nerek 293T (HEK293T) transfekowano pcDNA3.1-EPG. Uzupełniająca ryc. S4 pokazuje kolokalizację błony między markerem błony plazmatycznej pankadheryną (zielony) a ekspresją EPG (czerwony) w komórkach transfekowanych w porównaniu z nietransfekowanymi komórkami kontrolnymi Wykryliśmy większą kolokalizację w komórkach transfekowanych EPG w porównaniu z niestransfekowanymi komórkami kontrolnymi komórek, przy użyciu obu nakładających się Mandersa (EPG vs. kontrola: 0,36 vs. 0,32; wartość p = 0,024; Ryc. uzupełniający S4 ) i współczynniki korelacji Pearsona 41 (EPG vs. kontrola: 0,32 vs. 0,27; wartość p = 0,014; Rys. uzupełniający S4). Ponadto przeprowadzono stereotaktyczne wstrzyknięcia pAAV2-CaMKII::EPG-IRES-hrGFP do komory bocznej szczurów P1 (n = 10). Późniejsze immunobarwienie w pierwotnej korze somatosensorycznej przy użyciu poliklonalnego przeciwciała anty-EPG (rysunek uzupełniający S4 ) wykazało, że EPG może ulegać ekspresji in vivo .
Charakterystyka mechanistyczna EPG
Aby zrozumieć aktywność białka EPG in vitro na poziomie mechanistycznym, wygenerowaliśmy syntetyczny gen o tej samej sekwencji aminokwasowej EPG, ale zoptymalizowany pod kątem ekspresji bakteryjnej. Klonowaliśmy, eksprymowaliśmy i oczyszczaliśmy EPG na kolumnie z kobaltem i używaliśmy go do dalszych zastosowań. Dichroizm kołowy ujawnił słabe pasma alfa-helikalne przy długościach 208 i 222 nm, co wskazuje na niewielką ilość struktury alfa-helikalnej, potwierdzanej przez bioinformatykę. Gdy oczyszczone białko wystawiono na działanie statycznego pola magnetycznego (25 mT) nie zaobserwowano żadnych zmian konformacyjnych (rysunek uzupełniający S5). Wskazuje to, że mechanizm transdukcji EPG nie pociąga za sobą istotnych zmian w strukturze białka EPG. Ponadto nie wykryto żelaza, gdy oczyszczone białko poddano trawieniu trypsyną i chymotrypsyną, co sugeruje, że mechanizm magnetodetekcji nie jest zależny od skupisk żelazo-siarka w białku.
Charakterystyka EPG w komórkach ssaków
Komórki HEK293T transfekowano konstruktem lentiwirusa zawierającym EPG pod promotorem CMV (pLV-CMV::EPG-IRES-hrGFP), a obrazowanie wapnia przy użyciu fura-2/AM uzyskano dwa-trzy dni po transfekcji (ryc. 2A-C ). . Obliczono procentową zmianę w stosunku fura-2/AM przy wzbudzeniu 340/380 nm. Komórki poddano działaniu pola magnetycznego 50 mT przez 10 s indukowanego przez statyczny płaski magnes. Z n = 99 komórek GFP-dodatnich, 68 komórek wykazało znaczny wzrost [Ca2 + ]i. Średni wzrost intensywności fluorescencji [Ca2 + ]i wyniósł 232 ± 20% i wystąpił 13 ± 0,5 s po rozpoczęciu bodźca (Fig. 2D, E ). Dane w (rys. 2D) wykazują zmienną odpowiedź komórkową w komórkach HEK od pojedynczej transfekcji w odpowiedzi na stymulację magnetyczną. Nietransfekowane komórki nie wykazywały odpowiedzi na bodziec (n = 76). Aby określić, czy wzrost [Ca 2+ ]i był spowodowany zewnątrzkomórkowym pochodzeniem, komórki z ekspresją EPG obrazowano w roztworze do obrazowania zewnątrzkomórkowego bez Ca 2+ (n = 23) lub w roztworze do obrazowania pozakomórkowego bez Ca 2+ uzupełnionym z chelatorem Ca 2+ EGTA (n = 9). Bodziec magnetyczny spowodował średnie zmiany [Ca 2+ ]i o 81 ± 14% i 52,0 ± 3%, które były istotnie niższe w porównaniu z normalnymi warunkami ( F 4,219 = 27,47; p < 0,0001, jednoczynnikowa ANOVA). Następnie zbadaliśmy, czy uwalnianie wapnia z retikulum endoplazmatycznego (ER) jest wymagane w odpowiedziach za pośrednictwem EPG (n = 48). W komórkach wykazujących ekspresję EPG, które inkubowano z inhibitorem, tapsigarginą, bodziec magnetyczny nie wywoływał żadnych zmian [Ca2 + ]i (0,81 ± 1,95%) (Fig. 2F,G ). Wyniki te sugerują, że zarówno zewnątrzkomórkowe, jak i wewnątrzkomórkowe jony Ca2 + są uwalniane w odpowiedzi na statyczną stymulację magnetyczną EPG.
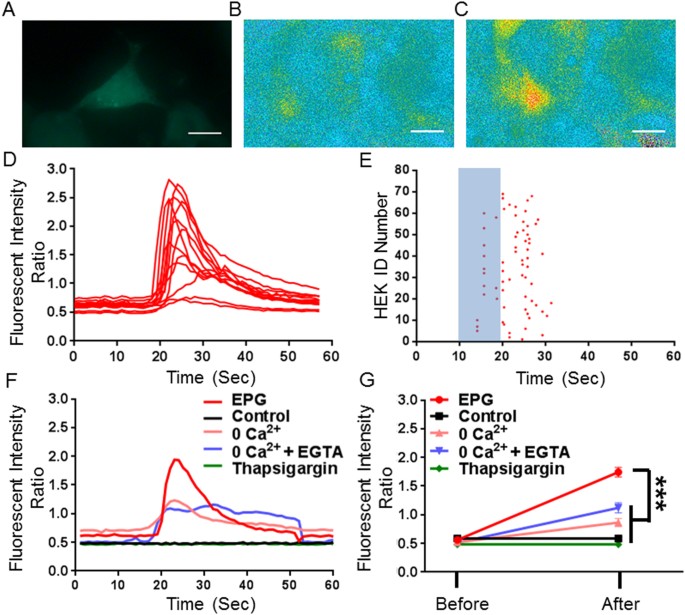
Stymulacja magnetyczna EPG w komórkach HEK293T wywołała znaczny wzrost [Ca2 +] i. ( A ) Komórki HEK293T transfekowane pLV-CMV-EPG-IRES-hrGFP. ( B , C ) Obrazy wapnia in vitro komórek obciążonych fura-2/AM przed ( B ) i po ( C ) 10 s stymulacji magnetycznej. Czarna strzałka wskazuje ciało komórki. Skala 10 µM. ( D ) Surowe dane pokazujące wzrost fluorescencji po stymulacji magnetycznej (niebieski słupek) w komórkach transfekowanych EPG. ( E ) Wykres rastrowy transfekowanych komórek odpowiadających na stymulację magnetyczną (czerwone kropki, n = 68). Komórki klasyfikowano jako odpowiadające, jeśli pik sygnału fluorescencji był 10 SD powyżej średniej. (F ) Dane pokazujące kinetykę odpowiedzi intensywności fluorescencji dla poszczególnych komórek w różnych warunkach. Zmniejszone zmiany intensywności fluorescencji zaobserwowano w 0 Ca 2+ i 0 Ca 2+ + EGTA po stymulacji magnetycznej. Nie zaobserwowano wzrostu sygnału dla komórek kontrolnych (nietransfekowanych) i traktowanych tapsygarginą. ( G ) Dane pokazujące średnie (±SEM) zmiany fluorescencji przed i po stymulacji magnetycznej dla każdego warunku n = 68 (EPG), n = 76 (Kontrola), n = 23 (0 Ca 2+ ), n = 9 ( 0 Ca 2+ + EGTA) & n = 48 (Thapsigargin). Jednoczynnikowa ANOVA, posttest Dunnetta (F4, 219) = 27,47, P < 0,0001.
Charakterystyka EPG w korowej hodowli neuronów
Neurony ze wspólnej hodowli korowej szczurów transdukowano konstruktem lentiwirusowym zawierającym EPG pod promotorem CMV (pLV-CMV::EPG-IRES-hrGFP). Kontrole mCherry przygotowano przez transfekcję neuronów konstruktem lentiwirusa pLV-CMV::IRES-mCherry. Siedem dni po transfekcji wykorzystaliśmy obrazowanie wapnia (fura-2/AM) do wizualizacji odpowiedzi neuronalnych. Po kokulturze chcieliśmy scharakteryzować naszą wspólną hodowlę neuronalną za pomocą specyficznych markerów neuronalnych (tubulina klasy III, tuj1) i glejowych (GFAP). Immunocytochemia wykazała, że kokultura wykazuje reaktywność immunologiczną na GFAP i TUJ1 (ryc. 3A, B ) w neuronach transfekowanych EPG ( ryc. 3C )potwierdzając, że kokultura składa się z pożądanej populacji neuronów glejowych wymaganej do tego badania. Pole magnetyczne było indukowane przez wykonany na zamówienie system elektromagnesów, który dostarczał impulsy o długości 5 ms z częstotliwością 10 Hz i indukował pole o wartości 50–70 mT. Figura 3E przedstawia pojedynczy neuron korowy transfekowany pLV-CMV::EPG-IRES-hrGFP wykazujący sygnał GFP w całym ciele komórki i procesach. Figura 3F przedstawia znakowanie neuronów EPG+ znakowaniem fura 2-AM po 1 godzinie. Figura 3G pokazuje, że stymulacja magnetyczna zwiększyła intensywność fura-2AM, wskazując na wzrost [Ca2 + ]i. Rysunek 3Hpokazuje surowe dane śladowe obrazowania fura 2-AM EPG wyrażających odpowiedzi neuronów na stymulację magnetyczną (niebieski pasek). Neurony EPG-dodatnie, które odpowiedziały na stymulację magnetyczną (n = 224) zostały wykreślone rastrowo w czasie; 77 neuronów z tej populacji (34%) odpowiedziało w ciągu 10 s stymulacji magnetycznej ( ryc. 3I ). Średni czas odpowiedzi wynosił 15 ± 0,5 s. Reprezentatywne odpowiedzi neuronów z ekspresją EPG, neuronów z ekspresją mCherry (kontrola), neuronów nietransfekowanych (kontrola) i neuronów z ekspresją EPG w różnych warunkach fizjologicznych, w tym roztwór zewnętrzny 0 Ca 2+, roztwór zewnętrzny 0 Ca 2+ + EGTA oraz z inhibitorem tapsigarginą , po stymulacji magnetycznej pokazano na ryc. 3J . Postać 3K pokazuje średnią procentową zmianę fluorescencji przed i po stymulacji magnetycznej. Jedynie neurony z ekspresją EPG wykazują wzrost fluorescencji fura-2AM po stymulacji magnetycznej. Stymulacja magnetyczna wywołała 144,8 ± 14,1% średni wzrost [Ca2 + ]i w neuronach z ekspresją EPG (n = 224; p < 0,0001). Nietransfekowane neurony kontrolne (0,50 ± 0,424%, n = 495) i neurony z ekspresją mCherry (0,14 ± 0,84%, n = 80) nie wykazały żadnej istotnej zmiany w odpowiedzi na bodziec. obrazowanie fura-2AM neuronów z ekspresją EPG inkubowanych z zewnętrznym 0 Ca 2+ (2 ± 0,98%, n = 475) oraz z 0 Ca 2+a EGTA (0,84 ± 0,64%, n = 175) nie wykazywały istotnych zmian w intensywności fluorescencji. Następnie inkubowaliśmy neurony eksprymujące EPG z blokerem pompy SERCA, tapsigarginą, w stężeniu 1 µM w 37°C przez 1 godzinę. Późniejsze obrazowanie neuronów nie spowodowało istotnej zmiany fluorescencji fura-2AM (0,50 ± 0,3%, n = 308). Razem, te wyniki pokazują, że zdalna aktywacja EPG w neuronach może indukować znaczny wzrost [Ca2 + ]i, wskazujący na pobudliwość neuronalną, tylko w neuronach eksprymujących EPG. Podobnie do wyników uzyskanych w komórkach HEK293T, hodowle neuronów wymagały fizjologicznych zewnątrzkomórkowych i wewnątrzkomórkowych poziomów wapnia, aby zareagować na stymulację magnetyczną. Rys. uzupełniający S6pokazuje, że zjawisko to zostało dodatkowo potwierdzone w hodowlach neuronów myszy, a także przy użyciu genetycznie kodowanego wskaźnika wapnia (GCaMP6). Ponadto chcieliśmy dodatkowo potwierdzić, że fluorescencja GFP neuronów EPG-dodatnich nie zakłóca fluorescencji fura-2/AM. Odkryliśmy, że komórki zawierające GFP (EPG pozytywne) mają taką samą fluorescencję fura-2/AM jak komórki nietransfekowane (rysunek uzupełniający S7 ). Zatem zastosowanie komórek transfekowanych EPG wyrażających GFP jako markera udanej transfekcji jest zgodne z zastosowaniem fura-2/AM do pomiaru wewnątrzkomórkowego [Ca2 + ].
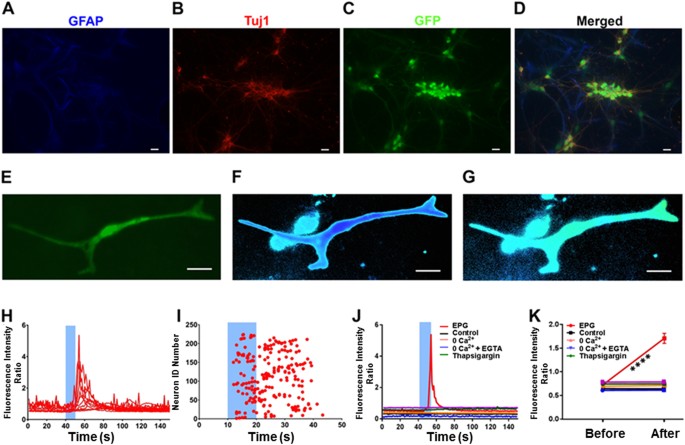
Immunocytochemia kokultury korowej i Magnetyczna stymulacja EPG w neuronach. (A) Komórki są pozytywne dla markerów neuronalnych i glejowych, takich jak (A) GFAP (niebieski), (B) Tuj1 (czerwony) w (C) EPG-dodatnie neurony (zielony). (D) Kolokalizacja neuronów EPG-dodatnich z GFAP i Tuj1. Pierwotne mieszane hodowle neuronów i gleju korowego transdukowano konstruktami wirusowymi dla EPG znakowanych GFP pod promotorem CMV (pLV-CMV::EPG-IRES-hrGFP). ( E – K ). (MI)Pierwotne mieszane hodowle neuronów i gleju korowego transdukowano konstruktami wirusowymi dla EPG znakowanych GFP pod promotorem CMV (pLV-CMV::EPG-IRES-hrGFP). Stransdukowane neurony obciążono wskaźnikiem wapnia fura-2 przed (F) i po (G) 10 s magnetyczna stymulacja EPG w neuronach indukuje znaczny wzrost [Ca2 + ]i, jak przedstawiono przez zmianę profilu intensywności. Przez 10 s stosowano przemienne statyczne pole magnetyczne (niebieski słupek). (H) Surowe dane pokazujące neurony transfekowane EPG ze wzrostem fluorescencji po stymulacji magnetycznej (niebieski słupek). (I) Wykres rastrowy transfekowanych komórek odpowiadających na stymulację magnetyczną (czerwone kropki, n = 225). (JOT)Dane pokazujące kinetykę odpowiedzi intensywności fluorescencji dla poszczególnych komórek w różnych warunkach. Zwiększone zmiany intensywności fluorescencji zaobserwowano w neuronach transfekowanych EPG po stymulacji magnetycznej. Różne warunki, takie jak O Ca 2+ (roztwór tyrodów z usuniętym Ca 2+ ), O Ca 2+ + EGTA, tapsigargina, mCherry i komórki nietransfekowane nie wykazują wzrostu sygnału po stymulacji magnetycznej. (K) Dane pokazujące średnie (±SEM) zmiany fluorescencji przed i po stymulacji magnetycznej dla każdego stanu n = 225 (EPG), n = 495 (kontrola), n = 475 (O Ca 2+ ), n = 175 ( O Ca 2+ + EGTA), n = 308 (Thapsigargin) & n = 80 (mCherry). Znaczący wzrost [Ca 2+]i w porównaniu z wartościami wyjściowymi zmierzono w neuronach eksprymujących EPG-GFP (*p < 0,0005, test t Studenta).
Bezprzewodowa aktywacja EPG w modelu gryzonia
Na koniec zajęliśmy się układem motorycznym kończyn gryzoni, który jest dobrze zbadanym obwodem ze zweryfikowanymi i wymiernymi testami aktywacji. Stereotaktyczną iniekcję wirusa zawierającego EPG (pAAV2-CaMKII::EPG-IRES-hrGFP) skierowano do neuronów ruchowych warstwy 5 w prawej pierwotnej korze ruchowej (M1) obszaru kończyn dorosłych szczurów (n = 10). Szczurom kontrolnym wstrzyknięto wirus zawierający tylko GFP (n = 5). Odpowiedzi na stymulację M1 mierzono za pomocą motorycznych potencjałów wywołanych (MEP) kończyn przednich dwa do trzech tygodni po wstrzyknięciach stereotaktycznych. Odpowiedzi MEP rejestrowano jednocześnie w prawej i lewej kończyny przedniej. Cewka TMS do dostarczania bodźca magnetycznego została umieszczona nad linią środkową głowy szczura ( ryc. 4A ). Wyjściowe odpowiedzi można zaobserwować w MEP kończyny przeciwnej u szczurów z ujemnym wynikiem EPG. Co więcej, MEP kończyny przeciwległej do kończyny, w której nie wykonano wstrzyknięcia, wykazuje odpowiedź wyjściową. U szczurów wykazujących ekspresję EPG w prawym M1 stymulacja bezprzewodowa indukowała odpowiedzi MEP w przeciwległej, lewej kończyny przedniej (0,39 ± 0,05 mV), które były znacznie większe niż odpowiedzi MEP zarejestrowane w prawej ipsilateralnej, przedniej kończyny (0,15 ± 0,04 mV, p < 0,005 , test t-Studenta) (rys. 4B ). U szczurów kontrolnych z ekspresją tylko GFP w prawym M1, stymulacja indukowała minimalną MEP w przeciwległej kończyny przedniej, która była znacząco mniejsza w porównaniu z grupą eksperymentalną (0,12 ± 0,03 mV, p < 0,001) i była podobna do odpowiedzi MEP obserwowanej w ipsilateralnej kończyna przednia (0,08 ± 0,01 mV, p > 0,30) (Rys. 4B ) . Średnie opóźnienie odpowiedzi wynosiło 11,3 ± 1 ms, co jest zgodne z raportami o opóźnieniach MEP zarejestrowanych innymi metodami stymulacji mózgu. Wyniki te pokazują, że bezprzewodowa aktywacja EPG daje większy, mierzalny wynik behawioralny in vivo .
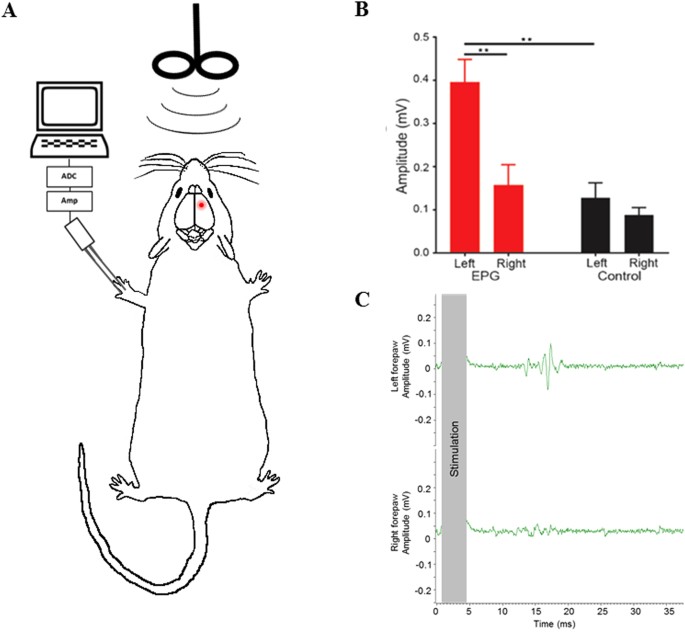
Bezprzewodowa stymulacja magnetyczna u szczurów z ekspresją EPG indukuje dużą odpowiedź mięśniową. (A) Karykatura przedstawiająca konfigurację in vivo . (B) Stymulacja magnetyczna kory spowodowała znaczny wzrost amplitudy odpowiedzi MEP w lewej kończyny przedniej szczurów z ekspresją EPG w prawym M1. Szczury kontrolne miały minimalne odpowiedzi MEP. (**p < 0,005) (C) Reprezentatywne ślady odpowiedzi MEP lewej (przeciwstronnej do EPG wyrażającej M1) i prawej (ipsilateralnej do EPG wyrażającej M1) odpowiedzi MEP kończyny przedniej na stymulację magnetyczną.
Dyskusja
Pole magnetyczne Ziemi waha się od 22 µT do 50 µT i jest najwyższe na biegunach, a najniższe wokół równika. Ponadto istnieją lokalne zmiany, a także efekty zewnętrzne spowodowane burzami magnetycznymi na Słońcu 42 , 43 . Wiele gatunków zwierząt potrafi wyczuwać niewielkie zmiany w polu magnetycznym 44 , cecha wyrafinowana ewolucyjnie do nawigacji i unikania drapieżników. Jednak mechanizmy umożliwiające odczuwanie magnetyczne są w dużej mierze nieznane.
Jednym z takich organizmów znanych od dziesięcioleci z reagowania na pola magnetyczne jest ryba K. bicirrhis . Tutaj wykazaliśmy, że K. bicirrhis wyczuwa zarówno statyczne, jak i zmienne pola magnetyczne. Zidentyfikowaliśmy EPG jako białko, które reaguje na EMF, chociaż dokładny mechanizm działania i sposób, w jaki aktywność EPG pośredniczy w zachowaniu K. bicirrhis, jest nieznany. Wcześniejsze pomiary wywołanych bodźcem zmian wewnątrzkomórkowego Ca 2+ z użyciem fura-2/AM w narządzie elektroreceptora bańkowego wykazały, że prąd transdukcyjny depolaryzuje błonę wierzchołkową i prowadzi do stymulacji presynaptycznych kanałów Ca 2+ i aktywacji synapsy 18. Odkrycie EPG sugeruje możliwy mechanizm transdukcji sygnału, który indukuje depolaryzację narządu elektroreceptorowego, a tym samym może ułatwić lepsze zrozumienie fizjologii ryb i zdolności wrażliwości elektromagnetycznej.
Bardzo interesujące jest zrozumienie mechanizmów, dzięki którym EPG wyczuwa sygnały magnetyczne i przekłada je na sygnały biochemiczne. Jest to szczególnie trudne, biorąc pod uwagę, że nie ma precedensu podobnego systemu biologicznego. Jednym ze sposobów badania struktury i funkcji EPG jest analiza bioinformatyczna. Analiza wykazała obecność reszt w domenie zewnątrzkomórkowej, które mogą ułatwiać interakcje białko-białko. Dlatego stawiamy hipotezę, że białko EPG może mieć pozakomórkowych partnerów wiążących. Prawdopodobnymi partnerami oddziałującymi innych członków domeny UPAR_LY6 są (a) domeny UPAR_LY6, (b) Kringle, (c) V-set, (d) Tiol_cytolizyna i (e) domeny Somatomedin_B 45. Ponieważ domena UPAR_LY6 może oddziaływać z innymi domenami UPAR_Ly6, białka EPG mogą tworzyć homo-oligomery z powodu oddziaływań między ich zewnątrzkomórkowymi domenami podobnymi do dysku, jak sugeruje dodatkowa ryc. S3 . Inne możliwe interakcje domeny UPAR_LY6 z domenami Kringle, Somatomedin-B i Ig-podobnymi V-set sugerują, że EPG może również oddziaływać z rozpuszczalnymi białkami w przestrzeni zewnątrzkomórkowej, jak również z białkami macierzy zewnątrzkomórkowej. W przypadku ekspresji w neuronach, zewnątrzkomórkowa domena UPAR_LY6 EPG może również wiązać się z fałdami Ig-podobnymi domen zewnątrzkomórkowych (domeny V-set) podjednostek beta 1 lub beta 2 kanałów sodowych bramkowanych napięciem 46 , 47 , 48 , 49. Brak jakiejkolwiek znanej domeny sygnalizacyjnej związanej z EPG prowadzi nas do przekonania, że EPG może działać głównie jako białko powierzchniowe komórki wiążące się z partnerami zewnątrzkomórkowymi lub domenami zewnątrzkomórkowymi pobliskich białek transbłonowych. Nasze wyniki pokazują, bioinformatyki przypuszczalne miejsca glikozylacji, które jest zgodne z jednym hipoteza sugeruje, że bicirrhis K. wyczuwać pole elektromagnetyczne poprzez glikozylowanych kanałów jonowych 50 . Alternatywnie, duża liczba reszt cysteiny może oznaczać, że EPG jest białkiem żelaza siarki 51 , nawet jeśli konwencjonalne wiązania żelaza nie zidentyfikowano i nasze badania biochemiczne nie wykazuje żadnych śladów żelaza. Ostatnio w białkach bogatych w aromatyczne aminokwasy u bakterii stwierdzono przewodnictwo metaliczne52 , 53 , a na koniec wykazano, że niskie pole magnetyczne wpływa na kinetykę enzymów bakteryjnych poprzez sprzężenie spinowo-orbitalne, gdy wiąże się on z gazem ksenonowym 54 . Dlatego należy zauważyć, że pełne wyjaśnienie działania EPG nie zostało jeszcze ustalone.
Oprócz zrozumienia biologicznych podstaw magnetosensacji istnieje duże zapotrzebowanie na nowe nieinwazyjne technologie neuromodulacji. Ostatnio doniesiono o próbach zdalnego sterowania produkcją białek in vivo za pomocą fal radiowych i ogrzewania pola magnetycznego nanocząstek żelaza 12 , 13 . Na przykład, ssaczy kanał wapniowy bramkowany temperaturą (TRPV1) sprzężony z transkrypcją genu insuliny zależną od wapnia został poddany bioinżynierii, aby był aktywowany falami radiowymi 11. Dwa ostatnie badania doniosły o inżynierii sztucznych chimerycznych magnetoczujników, w których kanały jonowe zostały połączone z ferrytyną, która jest wewnątrzkomórkowym białkiem przechowującym żelazo. Zaproponowano dwie główne teorie dotyczące wykrywania pola magnetycznego Ziemi: pierwsza opiera się na magnetycznych nanocząstkach, a druga polega na wykrywaniu za pomocą reakcji magnetochemicznej, w której różne rodzaje par rodników (różne w stanie spinu) powstają w obecności lub brak pola magnetycznego. Ostatnie badania sugerują połączenie dwóch mechanizmów, w których kompleks dwóch produktów genowych ( MagR , który tworzy magnetyczne nanokryształy i Cry , kryptochromowy fotoreceptor) tworzy „magnetyczny kompas” 55.. Jednak ten model zależy od obecności światła do aktywacji. Niemniej jednak, gdy powyżej magneto-czujniki podniesiony kontrowersji 56 . Inne badanie wskazuje na udział kanałów Kir4.2, BK i CaV1.3 w elektrodetekcji. Zgłoś one dwie cząsteczki mechanizm wykrywania w którym pary KCNJ15 / Kir4.2 z poliamin w wykrywanie słabych pól elektrycznych 57 . W przeciwieństwie do odbioru elektromagnetycznego, odbiór elektryczny opiera się na mechanizmie oddziaływania dodatnio naładowanych cząsteczek wewnątrzkomórkowych z kanałami K+ 57 . Wydaje się, że w obu przypadkach istnieje kanał K+, który jest aktywowany w odpowiedzi na drobne zmiany elektryczne 57 , 58. W jednym przypadku zachodzi potrzeba wiązania poliamin (sperminy i spermidyny) w celu spowolnienia aktywności kanału1, aw drugim występuje wstawienie 4 dodatnio naładowanych aminokwasów (KKKER)2. Opisane tutaj mechanizmy są nowe, chociaż należy zauważyć, że mogą występować różnice w wykrywaniu pola elektrycznego i magnetycznego Innym genem związanym z odpowiedzią na pole magnetyczne jest kanał jonowy bramkowany cyklicznym nukleotydem TAX-4 z nicienia Caenorhabditis elegans 16 . Różnice między tym genem a EPG sugerują, że różne organizmy opracowały alternatywne strategie ewolucyjne nawigacji zgodnie ze wskazówkami pól elektromagnetycznych.
Eksperymenty z obrazowaniem wapnia zarówno w komórkach HEK293T, jak i neuronach wyrażających EPG wykazały opóźnienie w odpowiedziach wapnia na stymulację magnetyczną rzędu kilku sekund. Nie jest wykluczone, że przy dalszym dostrajaniu parametrów stymulacji opóźnienie to może ulec skróceniu. Z drugiej strony może być tak, że technologia EPG nie jest zdolna do indukowania odpowiedzi neuronalnych rzędu milisekund; jeśli EPG jest białkiem związanym z błoną, które jest połączone z kanałem jonowym i/lub działa poprzez wtórne przekaźniki, aby wpływać na aktywność neuronalną, jego kinetyka może być rzędu sekund. Niemniej jednak, nawet przy opóźnieniach czasowych rzędu sekund, nieinwazyjna technologia, która umożliwi przejściową, specyficzną komórkowo i lokalizacyjną modulację aktywności neuronalnej, byłaby niezwykle potężna.
Z powodzeniem ekspresjonowaliśmy EPG w neuronach in vitro , a także ekspresjonowaliśmy EPG w mózgu szczura in vivo . W tym ostatnim przypadku obserwowaliśmy reakcje funkcji mięśni kończyny przedniej, gdy EPG wyrażane w korze ruchowej było zdalnie aktywowane. Dlatego aktywacja neuronów przez EPG daje wymierny wynik behawioralny. Odkrycie EPG jako domniemanego białka reagującego na EMF może otworzyć nowe możliwości zastosowania zdalnej kontroli aktywności komórkowej zarówno w ośrodkowym układzie nerwowym, jak i innych układach nieneuronalnych, w tym w sercu, mięśniach gładkich i szkieletowych oraz komórkach glejowych. Ponadto EPG może ulegać ekspresji pod różnymi promotorami, umożliwiając celowanie specyficzne dla komórki in vivo. W ten sposób technologia EPG może stanowić ekscytujące i cenne narzędzie do badania aktywności neuronalnej na poziomie sieciowym, komórkowym i molekularnym.
Materiały i metody
Wszystkie procedury na zwierzętach zostały przeprowadzone zgodnie z wytycznymi NIH Guide for the Care and Use of Laboratory Animals i zatwierdzone przez Komisję ds. Opieki nad Zwierzętami i Użytkowania na Uniwersytecie Johnsa Hopkinsa.
Eksperymenty behawioralne na rybach
Ryby K. bicirrhis trzymano w 30-galonowym zbiorniku, który utrzymywano w temperaturze 25°C. Poziomy amoniaku, azotynów i pH były testowane codziennie. Ryby karmiono 2–3 razy dziennie suchymi płatkami. Podczas eksperymentów zakryto boki zbiornika. Sesja behawioralna składała się z 8–10 pojedynczych prób, w tym prób kontrolnych z bodźcem pozorowanym. Udane próby charakteryzowały się odpływaniem ryb od pola elektromagnetycznego. Nagrania wideo z prób analizowano za pomocą oprogramowania Snagit11. Lokalizację i ruch ryb określono przy użyciu oprogramowania do oznaczenia końca ogona każdej ryby przed rozpoczęciem i podczas każdej sekundy próby.
Budowa biblioteki cDNA
Total mRNA was extracted from freshly dissected anal fins of 80 anesthetized glass catfish using the FastTrack 2.0 mRNA Isolation kit (Life Technologies). The cDNA library was constructed in pDONR222 using the CloneMiner II cDNA Library Construction kit (Life Technologies). The final cDNA library was cloned into pcDNA-DEST40 by LR recombination, transformed into One Shot TOP10 Chemically Competent cells (Life Technologies), and stored as glycerol stocks in 500 µL aliquots at −80 °C. The cDNA sub-libraries were constructed by replica plating. A 500 µL glycerol stock of the total cDNA library was added to 5 mL LB (Quality Biological) containing 100 mg/mL Ampicillin (Sigma-Aldrich) and shaken at 225 rpm, 37 °C for 1 hour. The total volume was evenly plated on ten 10-cm Ampicillin plates (Quality Biological) and incubated overnight at 37 °C. The following day, the ten plates were replica plated to a second set of ten plates using nitrocellulose membranes and each nitrocellulose membrane was submerged in a flask containing 50 mL LB. The plates and flasks were incubated overnight at 37 °C, cDNA sub-libraries were purified from the flasks’ inoculums, and glycerol stocks were prepared.
Produkcja cRNA
Podbiblioteczne i poszczególne cRNA transkrybowano stosując trawienie PmeI i zestaw mMESSAGE mMACHINE T7 ULTRA (Life Technologies). Po transkrypcji przeprowadzono reakcję ogonowania poli(A) i traktowanie DNazą I zgodnie z instrukcjami producenta. cRNA oczyszczono przez ekstrakcję fenol:chloroform, a następnie wytrącenie izopropanolem lub wytrącenie LiCl, a następnie rozpuszczono w wodzie wolnej od RNaz.
Mikroiniekcja oocytów i dwuelektrodowy zacisk napięcia
Podbiblioteczne i poszczególne cRNA przeszukiwano za pomocą dwuelektrodowego cęgowego napięcia (TEVC). Oocyty w stadium V/VI zebrane z Xenopus laevis, jak opisano wcześniej 59 , wstrzyknięto 10 do 200 ng cRNA i utrzymywano w 16°C w roztworze ND97 (w mM): 96 NaCl, 2 KCl, 1,8 CaCl 2 · 2 H 2 O, 1 MgCl 2 x 6 2O, 5 HEPES, pH 7,5/NaOH). Oocyty kontrolne wstrzyknięto 50 nl wody i inkubowano w ND97. Trzy dni po wstrzyknięciu wykonano TEVC (Clampex 9.2) przez nabicie dwóch elektrod (WPI) wypełnionych 3 M KCl o rezystancji < 1 MΩ. Nagrania były filtrowane dolnoprzepustowo przy 300 Hz. Oocyty utrzymywano na poziomie -40 mV przez 232 ms, a następnie zaciskano napięcie między -100 a 40 mV w krokach 20 mV trwających 1,6 ms każdy, a następnie przywracano do wartości -40 mV przez 230 ms (Oocyte Clamp OC-725A, Warner Instruments). Nagrania wykonano w różnych roztworach kąpieli zi bez stymulacji. Wszystkie eksperymenty prowadzono w temperaturze pokojowej (20–23 °C). Standardowy fizjologiczny roztwór zewnętrzny, ND96, zawierał (w mM) 96 NaCl, 2 KCl, 1,8 CaCl 2 ·2H 2 O, 1 mM MgCl 2 · 6H 20,5 mM HEPES, 2,5 mM pirogronian sodu, pH 7,5/NaOH. Analizę danych offline przeprowadzono na niestandardowym oprogramowaniu MATLAB (MathWorks).
Bioinformatyka
Kompleksowe poszukiwania dopasowań dla cDNA EPG z nienadmiarowym genomowym (nr/nt) i wyrażonymi znacznikami sekwencji (dbEST) przeprowadzono odpowiednio przy użyciu oprogramowania BLASTN i TBLASTX, stosując ustawienia domyślne. Sekwencja cDNA EPG została następnie poddana translacji in-silico przy użyciu narzędzia programowego EMBOSS translate (standardowy kod genetyczny) i przeszukana w bazie danych bez nadmiarowości białek (nr) przy użyciu DELTA-BLAST w celu zidentyfikowania konserwatywnych ewolucyjnie domen. Reprezentatywne białka powstałe w wyniku poszukiwań DELTA-BLAST i TBLASTX zostały wybrane do skonstruowania drzewa filogenetycznego białka EPG, ukazującego jego ewolucyjny związek z innymi białkami z tej samej nadrodziny. Drzewo filogenetyczne EPG wywnioskowano metodą maksymalnego prawdopodobieństwa opartą na modelu opartym na macierzy JTT przy użyciu oprogramowania MEGA6. Procent drzew, w których pokrewne taksony są skupione, jest pokazany obok gałęzi. Początkowe drzewo(a) do przeszukiwania heurystycznego uzyskano stosując metodę Neighbor-Joining do macierzy odległości parami oszacowanych przy użyciu modelu JTT. Drzewo jest narysowane w skali, a długość gałęzi mierzona jest liczbą substytucji na miejsce. Analiza obejmowała 55 sekwencji aminokwasowych. Wszystkie pozycje zawierające luki i brakujące dane zostały wyeliminowane. W ostatecznym zbiorze danych znalazły się łącznie 34 pozycje. Sekwencje aminokwasowe bliskich homologów EPG (wywnioskowane z drzewa filogenetycznego) zostały dopasowane przy użyciu MUSCLE (2.0) w celu przewidzenia przypuszczalnej struktury drugorzędowej białka EPG. Analizy TMHMM, J-Pred i Signal-Blast przeprowadzono na sekwencji aminokwasowej w celu zidentyfikowania drugorzędowej struktury sekwencji EPG. Przypuszczalną orientację EPG w błonie przewidziano przy użyciu oprogramowania Polyphobius. Wreszcie trzeciorzędowa struktura EPG została przewidziana przez modelowanie oparte na homologii przy użyciu oprogramowania SWISS-MODEL i została zwizualizowana przy użyciu DeepView.
Klonowanie EPG do ssaczych wektorów ekspresyjnych
Otwartą ramkę odczytu EPG sklonowano do pcDNA3.1D/V5-His-TOPO (Life Technologies) w celu oznaczenia EPG do wykrywania przeciwciał w testach biochemicznych (końcowy plazmid: pcDNA3.1-EPG-V5-His). W skrócie, startery do kierunkowego klonowania zawierające sekwencję KOZAK i kodon start zastosowano do amplifikacji PCR genu EPG i klonowania do wektora, zgodnie z instrukcjami produktu. cRNA zamplifikowano z tego plazmidu w celu sprawdzenia konserwatywnej funkcji EPG. W celu wirusowej ekspresji EPG w skrawkach mózgu, EPG trawiono z pcDNA3.1-EPG-V5-His i ligowano do miejsca wielokrotnego klonowania pAAV-IRES-hrGFP (Agilent) przy użyciu miejsc BamHI i XhoI .
Analiza RT-PCR
Całkowite RNA wyekstrahowano z tkanki rybnej przy użyciu zestawu Quick-RNA Mini Prep (Zymo Research). Pierwsza nić cDNA została zsyntetyzowana przy użyciu zestawu do syntezy cDNA iScript i starterów oligo dT (BioRad) zgodnie z instrukcjami producenta. Test odwrotnej transkrypcji-PCR (RT-PCR) został zaprojektowany do wykrywania ekspresji mRNA rybiego EPG. Do przodu 5′-CGA TCG CGG AGT CTC TTA CC-3′ i do tyłu 5′-CGG GGT TGC AGT TGT TTG TG-3′ zastosowano jako oligonukleotydy o następujących parametrach cyklu: (1) 2 min gorącego startu w 96°C (2) 35 cykli po 1 min w 94°C, 45 s w 55°C i 1 min w 72°C (4) wydłużanie w 72°C przez 15 min.
Produkcja wirusa związanego z adenowirusem (AAV)
AAV o wysokim mianie wytworzono przy użyciu systemu AAV Helper-Free System (Agilent) i zagęszczono przy użyciu zestawu AAV Purification Maxi (Biomiga). Dla miana wirusa (~1 × 10 6 − 1 × 10 9 TU/ml), 10-krotne seryjne rozcieńczenia wirusa transdukowano do komórek HEK293T wysianych w 70-80% konfluencji na 24-studzienkowych płytkach, a komórki o zielonej fluorescencji zliczano 4 dni po zakażeniu. Nieskoncentrowany wirus o niskim mianie wytworzono stosując tę samą procedurę transfekcji, co w przypadku wirusa o wysokim mianie. 72 godziny po transfekcji, komórki i supernatant zebrano i trzykrotnie zamrożono i rozmrożono, odwirowano przy 4000 obr./min w 4°C przez 15 min, przesączono w kolbie filtracyjnej 0,45 µm (Millipore) i przechowywano jako porcje 1 ml w - 80 °C. Ponadto, AAV niosący EPG pod specyficznym dla neuronów pobudzających promotorem CaMKII (AAV2-CamKIIa-EPG-IRES-hrGFP) został wykonany na zamówienie przez Vector Biolabs. Zainfekowane komórki można było zidentyfikować na podstawie pozytywnej ekspresji GFP. Pierwotne miano wirusa 1,9 × 10^13 zostało rozcieńczone 1000 razy przed podaniem do studzienek z hodowlą komórkową.
Niestandardowa produkcja lentiwirusa (LV)
Lentiwirusa zawierający promotor CMV :: EPG IRES hrGFP i PLV CMV :: IRES mCherry kontroli był zwyczaj wytwarzana z Cyagen (Guangzhou Biosciences Inc.) w funkcjonalnym miana 3,57 ± 2 x 10 9 TU / ml.
Niestandardowa produkcja przeciwciał EPG
W Genscript, NY, wytworzono niestandardowe przeciwciało poliklonalne anty-EPG. Analiza sekwencji aminokwasowej białka EPG wykazała, że fragment pomiędzy pozycjami aminokwasowymi 21 i 133 (AA21–AA133) był immunogenną częścią białka (OptymumAntigen™ Design Program firmy GenScript). Po usunięciu N-końcowego peptydu sygnałowego (AA1–AA20) fragment białka (AA21–AA133) ulegał ekspresji w systemie bakteryjnym. Wyrażone białko następnie oczyszczono i zastosowano do immunizacji dwóch królików nowozelandzkich przy użyciu konwencjonalnego protokołu immunizacji. Po 3 rundach immunizacji, skrwawienia produkcyjne od dwóch królików oczyszczono oddzielnie przez powinowactwo w celu wyizolowania przeciwciał poliklonalnych. Wyizolowane przeciwciała były następnie testowane jakościowo za pomocą pośredniego testu ELISA.
Immunocytochemia, kolokalizacja i analiza statystyczna
Komórki HEK293T transfekowano pcDNA3.1 EPG przy użyciu odczynnika Lipofectamine 2000 (Life Technologies, Inc.) i hodowano na szklanych szkiełkach pokrytych poli-L-lizyną (PLL; Sigma-Aldrich). Komórki kontrolne nie były transfekowane. W skrócie, komórki płukano PBS 48 h po transfekcji, utrwalano w 4% paraformaldehydzie przez 30 min, płukano trzykrotnie DPBS i blokowano w 5% NGS w PBS przez 1 godzinę. Komórki permeabilizowano 0,2% Triton X-100 (Sigma-Aldrich) przez 5 minut, ponownie płukano i dwukrotnie barwiono mysim przeciwciałem przeciw Pan Cadherin 1:100 (Sigma-Aldrich) i 1:50 zrobionym kostiumowym króliczym przeciwciałem przeciw EPG przez noc o 4:00 °C. Następnie komórki ponownie przemyto i inkubowano w 1:500 koziej anty-mysiej Alexa 488 i koziej anty-króliczej Alexa 568 (Life Technologies, Inc.) przez 1 godzinę. Jądro barwiono DAPI (25 ng/ml, Sigma-Aldrich) przez 10 min.
W celu określenia, czy EPG jest zlokalizowane w błonie komórkowej, mamy wspólną ekspresję EPG z immunobarwieniem błonowym. Współlokalizację obrazów konfokalnych między dwoma kanałami w komórkach transfekowanych HEK293T w porównaniu z nietransfekowanymi komórkami kontrolnymi mierzono przy użyciu oprogramowania Huygens Essential (SVI Huygens, Holandia). Określiliśmy ilościowo liczbę pikseli, które miały zarówno kolor zielony (pankadheryna, plama na błonie), jak i czerwony (anty-EPG). Wykorzystano dwa różne testy statystyczne, współczynniki korelacji Overlapping i Pearsona, aby uzyskać informacje ilościowe o stopniu nakładania się przestrzennego między dwoma kanałami.
Obrazowanie wapnia w komórkach HEK293T
Komórki HEK293T transfekowano pLENTI-CMV::EPG-IRES-hrGFP (4 μg) i Lipofectamine 2000 (Invitrogen) zgodnie ze standardowymi protokołami. Transfekowane komórki inkubowano przez 48 godzin w 37°C przed obrazowaniem. Obrazowanie wapnia przeprowadzono z transfekowanych komórek wysianych na płytki szklane i nakrywkowych inkubowano przez noc w inkubatorze w wilgotnej atmosferze utrzymywano w temperaturze 37 ° C, 10% CO 2 . Komórki płukano trzykrotnie roztworem do obrazowania wapnia (CIS) (125 mM NaCl, 2 mM MgCl2, 4,5 mM KCl, 10 mM Glukoza, 20 mM HEPES i 2 mM CaCl 2 doprowadzone do pH 7,4 (bez dodatku CaCl 2 dla Ca 2+bufor ad zastąpiono jonami Na). Komórki te ładowano 1 μM fura-2-AM przez 45 min w 37°C. Komórki następnie przemyto trzykrotnie CIS i deestryfikowano przez 30 min w 37°C. Szalki hodowlane zostały następnie załadowane do dostosowanych komór obrazowania i zobrazowane. Komórki GFP-dodatnie wybrano losowo z pola obrazu. Bodziec magnetyczny był dostarczany za pomocą magnesów statycznych o polu magnetycznym 50 mT przez okres 10 sekund. Dane określono ilościowo jako zmiany fluorescencji w czasie po stymulacji magnetycznej. Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji.
Immunohistochemia
Cortical mixed glial cultures were prepared from P0-P2 ICR (CD-1®; Harlan Laboratories) rat pups. Neuron-glia co-cultures were maintained in complete Neurobasal medium. On Day 4 cells were infected with plenti virus containing the CMV::EPG- GFP and un-infected cells served as control.
W celu scharakteryzowania wspólnej hodowli neuronów, jako marker neuronalny zastosowano króliczą poliklonalną antyneuronalną klasę III β-tubulinę (Biolegend; rozcieńczenie 1:500), mysie monoklonalne anty-GFAP (Dako; rozcieńczenie 1:500) jako marker glejowy i kurze anty GFP (abcam; rozcieńczenie 1:200). Po całonocnej inkubacji szkiełka nakrywkowe dokładnie przemyto DPBS i inkubowano odpowiednio w ośle anty-mysim Alexa 405 (abcam), kozim anty-króliczym Alexa 594 i kozim anty-kurzym Alexa 488 (Thermofisher Scientific), odpowiednio w rozcieńczeniach 1:500 przez 1 godzinę . Obrazy uzyskano przy użyciu pionowego mikroskopu epifluorescencyjnego M2 AxioImager (Carl Zeiss, Oberkochen, Niemcy) wyposażonego w moduł Apotome i obiektywy 10 × /0,45 NA i 20 × /0,8 NA i przetworzono przy użyciu AxioVision, wersja 4.8 (Carl Zeiss).
Pierwotna hodowla neuronów korowych i obrazowanie wapnia
Mieszane kultury glejowe korowe przygotowano z młodych szczurów P0-P2 (Harlan Laboratories). Korę wycięto, zmielono i inkubowano z trypsyną (2,5 mg/ml; Sigma, St. Louis, MO) i DNazą (0,015 mg/ml; Sigma) w 10 ml DMEM (Invitrogen) z 25 µM glutaminianem (30 min. 37°C). Tkankę roztarto, ponownie zawieszono w 10 ml glejowej pożywki podtrzymującej wykonanej z DMEM z 10% płodową surowicą bydlęcą (Hyclone, Logan, UT) i komórki przesączono dwukrotnie przez nylonową siatkę o porach 70 μm. Komórki wysiano i zmieniono pożywkę 24 godziny po wysianiu, a następnie co 2-3 dni. Neurony korowe przygotowano z zarodków szczurzych E18 (Harlan Laboratories). Korę wycięto, zmielono i inkubowano z trypsyną i DNazą w 10 ml pożywki Neurobasal uzupełnionej B27 (Invitrogen) i 200 nM L-glutaminy (Invitrogen) (30 min, 37 °C). Tkankę roztarto, ponownie zawieszono w 10 ml uzupełnionej pożywki Neurobasal i komórki przesączono dwukrotnie przez nylonową siatkę o porach 70 μm. Neurony umieszczono na wierzchu zlewnej warstwy mieszanego złoża glejowego przy gęstości 0,8–1,0 × 10^5 komórek na studzienkę. Wspólne hodowle Neuron-gleju utrzymywano w kompletnej pożywce Neurobasal. W dniu 5 komórki zakażono lentiwirusem zawierającym CMV::EPG-IRES-hrGFP lub pLV-CMV::IRES-mCherry jako kontrolę. Inne komórki kontrolne pozostały niezakażone. Komórki inkubowano w 37°C przez 3 dni po zakażeniu. Hodowle gleju neuronalnego załadowano 1 μM fura-2/AM (Molecular Probes/Invitrogen; 45 min, 37 °C) w roztworze Tyrodesa (119 mM NaCl, 5 mM KCl, 25 mM HEPES bufor, 2 mM CaCl2, 2 mM MgCl2, 6 g/litr glukozy, dostosować pH do 7. 4 z NaOH), a następnie inkubowano przez dodatkowe 30 min w 37°C, aby umożliwić całkowitą hydrolizę acetoksy-metylowej grupy estrowej. Do obrazowania zmian fluorescencyjnych proporcjonalnych do wewnątrzkomórkowego stężenia wapnia podczas stymulacji zastosowano odwrócony mikroskop Olympus 1 × 71 z podwójną kondensorową kolumną oświetleniową. Obliczono procentową zmianę stosunku fura-2 przy wzbudzeniu 340/380 nm względem wartości zarejestrowanych w t = 0 dla każdego neuronu. Bodziec magnetyczny był dostarczany za pomocą elektromagnesu o polu magnetycznym 50 mT przez okres 10 sekund. Dane określono ilościowo jako zmiany fluorescencji w czasie po stymulacji magnetycznej. Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 Ca Do obrazowania zmian fluorescencyjnych proporcjonalnych do wewnątrzkomórkowego stężenia wapnia podczas stymulacji zastosowano odwrócony mikroskop Olympus 1 × 71 z podwójną kondensorową kolumną oświetleniową. Obliczono procentową zmianę stosunku fura-2 przy wzbudzeniu 340/380 nm względem wartości zarejestrowanych w t = 0 dla każdego neuronu. Bodziec magnetyczny był dostarczany za pomocą elektromagnesu o polu magnetycznym 50 mT przez okres 10 sekund. Dane określono ilościowo jako zmiany fluorescencji w czasie po stymulacji magnetycznej. Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 Ca Do obrazowania zmian fluorescencyjnych proporcjonalnych do wewnątrzkomórkowego stężenia wapnia podczas stymulacji zastosowano odwrócony mikroskop Olympus 1 × 71 z podwójną kondensorową kolumną oświetleniową. Obliczono procentową zmianę stosunku fura-2 przy wzbudzeniu 340/380 nm względem wartości zarejestrowanych w t = 0 dla każdego neuronu. Bodziec magnetyczny był dostarczany za pomocą elektromagnesu o polu magnetycznym 50 mT przez okres 10 sekund. Dane określono ilościowo jako zmiany fluorescencji w czasie po stymulacji magnetycznej. Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 Ca Obliczono procentową zmianę stosunku fura-2 przy wzbudzeniu 340/380 nm względem wartości zarejestrowanych w t = 0 dla każdego neuronu. Bodziec magnetyczny był dostarczany za pomocą elektromagnesu o polu magnetycznym 50 mT przez okres 10 sekund. Dane określono ilościowo jako zmiany fluorescencji w czasie po stymulacji magnetycznej. Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 Ca Obliczono procentową zmianę stosunku fura-2 przy wzbudzeniu 340/380 nm względem wartości zarejestrowanych w t = 0 dla każdego neuronu. Bodziec magnetyczny był dostarczany za pomocą elektromagnesu o polu magnetycznym 50 mT przez okres 10 sekund. Dane określono ilościowo jako zmiany fluorescencji w czasie po stymulacji magnetycznej. Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 Ca Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 Ca Transfekowane komórki traktowano tapsigarginą (Sigma T9033) w stężeniu 1 μM, a następnie obrazowano 1 godzinę po inkubacji. Do doświadczeń bez wapnia 0 CaUżyto opon 2+ . W doświadczeniach z dodatkowym zewnętrznym buforowaniem Ca2 + zastosowano 3 Mm EGTA.
Obrazowanie EPG-GCaMP6
Wspólne hodowle neuronów-gleju myszy utrzymywano w kompletnej pożywce Neurobasal. W dniu 5 komórki zakażono wirusem AAV2 zawierającym CaMKII::EPG-GFP lub tylko CaMKII::GFP jako kontrolę. Inne komórki kontrolne pozostały niezakażone. Komórki inkubowano w 37°C przez 3 dni po zakażeniu. Hodowle Neurona-glia załadowano 1 μM fura-2/AM (MolecularProbes/Invitrogen; 45 min, 37 °C) w zrównoważonym roztworze soli Hanka z 10 mM buforem HEPES (pH 7,2), a następnie inkubowano przez dodatkowe 30 min w 37 °C, aby umożliwić całkowitą hydrolizę acetoksy-metylowej grupy estrowej. Zmiany w [Ca 2+]i wykryto również przy użyciu genetycznie kodowanych czujników wapnia, AAV5-Syn::GCaMP6s-WPRE-SV40 (Penn vector lab, Filadelfia, PA). Po umożliwieniu dojrzewania kultur neuronów glejowych przez 5 dni, wektor wirusowy GCaMP 6s podano do końcowego stężenia 1 × 10^6 cząstek wirusowych/ml. Neurony obrazowano osiem dni po transfekcji. Do obrazowania zmian fluorescencyjnych proporcjonalnych do wewnątrzkomórkowego stężenia wapnia podczas stymulacji zastosowano odwrócony mikroskop Olympus 1 × 71 z podwójną kondensorową kolumną oświetleniową. Obliczono procentową zmianę stosunku fura-2 przy wzbudzeniu 340/380 nm względem wartości zarejestrowanych w t = 0 dla każdego neuronu. Neurony GFP-dodatnie, których stymulacja wywołała wzrost uśrednionych stosunków fura-2 o co najmniej jedno odchylenie standardowe, uznano za reagujące.
Stereotaktyczny wstrzyknięcie AAV w mózg szczura
Dorosłe szczury Sprague-Dawley otrzymały stereotaktyczną iniekcję wirusa AAV2 kodującego EPG pod promotorem CaMKII (pAAV2-CaMKII::EPG-IRES-hrGFP) (n = 10) lub AAV2 kodującego tylko GFP (pAAV2-CaMKII::IRES-hrGFP) (kontrola, n = 5). Operacje przeprowadzono w znieczuleniu izofluranem. Igłę do mikroiniekcji umieszczono w prawej M1 do docelowej kończyny przedniej (AP: + 1,6 mm, ML: +3,0 mm, DV: -1,7 mm) i wstrzyknięto 3 µl AAV2. Ponadto szczurom P1 Sprague-Dawley wstrzyknięto stereotaktycznie 1 µl wirusa AAV kodującego EPG lub GFP w prawej komorze bocznej ( n = 10; przednio-tylne, 0,8 mm, przyśrodkowo-boczne, 2 mm, grzbietowo-brzuszne, 1,8 mm) według Li i in . 7 . Szczury umieszczono w aparacie stereotaktycznym pod krioanestezją.
Immunohistochemia wycinków mózgu
Cztery tygodnie po stereotaktycznym wstrzyknięciu wirusa do komór bocznych w wieku P1, P30, szczurom, którym wstrzyknięto P30 i grupie kontrolnej, której nie wstrzyknięto w tym samym wieku, poddano perfuzji odpowiednio 4% paraformaldehydem (zimny lód) i 10% roztworem formaliny (w temperaturze pokojowej). Swobodnie pływające 50 µm skrawki inkubowano z przeciwciałem poliklonalnym anty-EPG przez 48 godzin w temperaturze 4°C. Skrawki następnie przemyto i inkubowano z biotynylowanym drugorzędowym przeciwciałem (Vector Laboratories, CA) przez 1 godzinę w temperaturze pokojowej. Skrawki następnie poddano obróbce do barwienia niklem-3,3'-diaminobenzydyną (Ni-DAB) przy użyciu Vectastain Elite (Vector Laboratories) 60 . Przekroje zobrazowano w AxioImager M2 (Carl Zeiss AG) przy użyciu oprogramowania Axiovision Rel 4.8 do akwizycji obrazu.
Pomiary potencjału wywołanego silnika in vivo
Dorosłe szczury wyrażające EPG ukierunkowane na neurony L5 w korze ruchowej początkowo znieczulano izofluranem, a następnie znieczulenie utrzymywano deksmedetomidyną (0,1 mg/kg/godz. sc). Szczurom wszczepiono elektrody do elektromiografii (EMG) do obustronnego bicepsa (Natus, Pleasanton, CA). Cewka TMS została umieszczona nad głową, a środek cewki znajdował się na środku obustronnej kory ruchowej. Około 75% mocy stymulatora było wymagane do wywołania spoczynkowego progu motorycznego mięśnia bicepsa szczura. Aby zmaksymalizować wykrywanie MEP indukowanego TMS, w całym eksperymencie zastosowano maksymalną moc wyjściową maszyny przy 100% (około 30% progu spoczynkowego motoryki). Rejestrację elektromiograficzną wykonano z następującymi specyfikacjami: filtr górnoprzepustowy przy 5 kHz, filtr dolnoprzepustowy przy 500 Hz, częstotliwość próbkowania przy 25 kHz.3 (FHC, Bowdoin, ME), a dane zebrano przy użyciu jednostki akwizycji danych Micro1401-3 (CED, Cambridge, UK). Za pomocą oprogramowania Spike 2 (CED, Cambridge, Wielka Brytania) zmierzono amplitudy i opóźnienie motorycznych potencjałów wywołanych. Amplitudę określono jako wysokość od ujemnego piku do najwyższego piku, a latencję zdefiniowano jako punkt czasowy, w którym początkowy pik wystąpił po bodźcu. Dla każdego zwierzęcia obliczono średnie z dziesięciu przemiatań.
Stymulacja magnetyczna
Natężenie pola magnesu mierzono konsekwentnie przed eksperymentami wymagającymi stymulacji. W tym celu wykorzystaliśmy miernik Gaussa. Przed rozpoczęciem eksperymentów ze stymulacją ryb użyliśmy linijki do pomiaru odległości między rybą a źródłem stymulacji magnetycznej i wielokrotnie mierzyliśmy natężenie pola za pomocą gausomierza. Informujemy, że nasze wartości były spójne. W przypadku eksperymentów obejmujących stymulację komórkami HEK i neuronami korowymi pole magnetyczne było indukowane przez wykonany na zamówienie system elektromagnesów, który dostarczał impulsy 5 ms z częstotliwością 10 Hz i indukował pole o wartości 50–70 mili tesli. Elektromagnes był trzymany i pozycjonowany za pomocą systemu manipulatora. Komórki w naczyniu umieszczano najpierw pod mikroskopem, a następnie mierzono natężenie pola elektromagnesu gaussometrem z odległości 1 cm. Cewka elektromagnetyczna jest zdalnie sterowana przez wejście elektryczne. Wyłączamy wejście i powoli ustawiamy cewkę elektromagnetyczną nad polem ogniw. Ustaliliśmy, że odległość między elektromagnesem a ogniwami wynosi 1 cm. Następnie włączamy bodziec na okres 10 sekund.
Statystyka
Wyniki i liczby przedstawiają średnią ± błąd standardowy średniej (SEM). W stosownych przypadkach stosowano dwustronny test t Studenta i ANOVA (o ile nie stwierdzono inaczej).
Dostępność danych
Zbiory danych wygenerowane podczas i/lub przeanalizowane podczas bieżącego badania są dostępne u odpowiedniego autora na uzasadnione żądanie.
Bibliografia
- 1.
Boyden, ES, Zhang, F., Bamberg, E., Nagel, G. & Deisseroth, K. Milisekundowa skala czasu, genetycznie ukierunkowana optyczna kontrola aktywności neuronalnej. Nat Neurosci 8 , 1263-1268 (2005).
- 2.
Gradinaru, V., Thompson, KR i Deisseroth, K. eNpHR: halorodopsyna Natronomonas wzmocniona do zastosowań optogenetycznych. Brain Cell Biol 36 , 129-139 (2008).
- 3.
Han, X. i in . Optyczna kontrola dynamiki neuronalnej w skali milisekundowej w mózgu naczelnych innych niż człowiek. Neuron 62 , 191-198 (2009).
- 4.
Wang, H. i in . Szybkie mapowanie połączeń synaptycznych za pomocą fotostymulacji u transgenicznych myszy Channelrhodopsin-2. Proc Natl Acad Sci USA 104 , 8143-8148 (2007).
- 5.
Aravanis, AM i in . Optyczny interfejs neuronowy: kontrola in vivo kory ruchowej gryzoni za pomocą zintegrowanej technologii światłowodowej i optogenetycznej. J Neural Eng 4 , S143-156 (2007).
- 6.
Gradinaru, V., Mogri, M., Thompson, KR, Henderson, JM & Deisseroth, K. Optyczna dekonstrukcja parkinsonowskich obwodów neuronowych. Nauka 324 , 354-359 (2009).
- 7.
Li, N. i in . Plastyczność korowa kierowana optogenetycznie po uszkodzeniu nerwu. Proc Natl Acad Sci USA 108 , 8838-8843 (2011).
- 8.
Alexander, GM i in . Zdalna kontrola aktywności neuronalnej u myszy transgenicznych z ekspresją wyewoluowanych receptorów sprzężonych z białkiem G. Neuron 63 , 27-39 (2009).
- 9.
Coward, P. i in . Sterowanie sygnalizacją za pomocą specjalnie zaprojektowanego receptora sprzężonego z Gi. Proc Natl Acad Sci USA 95 , 352-357 (1998).
- 10.
Zemelman, BV, Nesnas, N., Lee, GA i Miesenbock, G. Bramkowanie fotochemiczne heterologicznych kanałów jonowych: zdalna kontrola nad genetycznie wyznaczonymi populacjami neuronów. Proc Natl Acad Sci USA 100 , 1352-1357 (2003).
- 11.
Stanley, SA i in . Ogrzewanie za pomocą fal radiowych nanocząstek tlenku żelaza może regulować poziom glukozy w osoczu u myszy. Nauka 336 , 604–608 (2012).
- 12.
Huang, H., Delikanli, S., Zeng, H., Ferkey, DM & Pralle, A. Zdalne sterowanie kanałami jonowymi i neuronami poprzez ogrzewanie nanocząstek polem magnetycznym. Nat Nanotechnol 5 , 602-606 (2010).
- 13.
Chen, R., Romero, G., Christiansen, MG, Mohr, A. & Anikeeva, P. Bezprzewodowa magnetotermiczna głęboka stymulacja mózgu. Nauka 347 , 1477-1480 (2015).
- 14.
Ibsen, S., Tong, A., Schutt, C., Esener, S. & Chalasani, SH Sonogenetics to nieinwazyjne podejście do aktywacji neuronów w Caenorhabditis elegans. Nat Commun 6 , 8264 (2015).
- 15.
Long, X., Ye, J., Zhao, D. & Zhang, S.-J. Magnetogenetyka: zdalna nieinwazyjna aktywacja magnetyczna aktywności neuronalnej za pomocą magnetoreceptora. Nauka. Bull ., 1-13 (2015).
- 16.
Vidal-Gadea, A. i in . Neurony magnetoczułe pośredniczą w orientacji geomagnetycznej u Caenorhabditis elegans. Życie 4 (2015).
- 17.
Lissmann, HW & Machin, KE Receptory elektryczne w rybach nieelektrycznych (Clarias). Naturę 199 , 88-89 (1963).
- 18.
Struik, ML, Steenbergen, HG, Koster, AS, Bretschneider, F. & Peters, RC Jednoczesne pomiary mobilizacji wapnia i aktywności nerwów aferentnych w narządach elektroreceptorowych znieczulonego Kryptopterus bicirrhis. Por. Biochem Physiol A Mol Integr Physiol 130 , 607-613 (2001).
- 19.
Caterina, MJ i in . Receptor kapsaicyny: aktywowany ciepłem kanał jonowy w szlaku bólu. Naturę 389 , 816-824 (1997).
- 20.
Preston, GM, Jung, JS, Guggino, WB & Agre, P. Reszta wrażliwa na rtęć przy cysteinie 189 w kanale wodnym CHIP28. J Biol Chem 268 , 17-20 (1993).
- 21.
Wachtel, AW & Szamier, RB Specjalne skórne narządy receptorowe ryb. IV. Narządy bańkowe suma nieelektrycznego, Kryptopterus. J Morfhol 128 , 291-308 (1969).
- 22.
Nagel, G. i in . Channelrodopsyna-1: bramkowany światłem kanał protonowy w zielonych algach. Nauka 296 , 2395-2398 (2002).
- 23.
Schroeder, BC, Cheng, T., Jan, YN i Jan, LY Klonowanie ekspresyjne TMEM16A jako podjednostki kanału chlorkowego aktywowanego wapniem. Komórka 134 , 1019-1029 (2008).
- 24.
McEntyre, J. & Ostell, J. Podręcznik NCBI. (2002).
- 25.
Rice, P., Longden, I. & Bleasby, A. EMBOSS: europejski otwarty pakiet oprogramowania do biologii molekularnej. Trendy w genetyce 16 , 276–277 (2000).
- 26.
Jones, DT, Taylor, WR & Thornton, JM Szybkie generowanie macierzy danych mutacji z sekwencji białek. Zastosowania komputerowe w naukach biologicznych: CABIOS 8 , 275–282 (1992).
- 27.
Edgar, RC MUSCLE: wielokrotne dopasowanie sekwencji z wysoką dokładnością i wysoką przepustowością. Kwasy nukleinowe badania 32 , 1792-1797 (2004).
- 28.
Edgar, RC MUSCLE: metoda dopasowania wielu sekwencji o zmniejszonej złożoności czasowej i przestrzennej. Bioinformatyka BMC 5 , 113 (2004).
- 29.
Drozdetskiy, A., Cole, C., Procter, J. & Barton, GJ JPred4: serwer przewidywania struktury drugorzędowej białka. Badania kwasów nukleinowych , gkv332.
- 30.
Kall, L., Krogh, A. & Sonnhammer, EL Tylny dekoder HMM do przewidywania cech sekwencji, który zawiera informacje o homologii. Bioinformatyka (Oxford, Anglia) 21 (Suppl 1), i251–257 (2005).
- 31.
Sonnhammer, ELL, Von Heijne, G. & Krogh, A. Ukryty model Markowa do przewidywania helis transbłonowych w sekwencjach białkowych. W Ismb , tom. 6, 175-182 (1998).
- 32.
Frank, K. & Sippl, MJ Wysokowydajne przewidywanie peptydów sygnałowych w oparciu o techniki dopasowywania sekwencji. Bioinformatyka (Oxford, Anglia) 24 , 2172-2176 (2008).
- 33.
Biasini, M. i in . SWISS-MODEL: modelowanie trzeciorzędowej i czwartorzędowej struktury białek z wykorzystaniem informacji ewolucyjnych. Badania kwasów nukleinowych 42 , W252–258.
- 34.
Arnold, K., Bordoli, L., Kopp, J. & Schwede, T. Przestrzeń robocza SWISS-MODEL: środowisko internetowe do modelowania homologii struktury białek. Bioinformatyka (Oxford, Anglia) 22 , 195-201 (2006).
- 35.
Kiefer, F., Arnold, K., Kunzli, M., Bordoli, L. & Schwede, T. Repozytorium SWISS-MODEL i powiązane zasoby. Badania kwasów nukleinowych 37 , D387-392 (2009).
- 36.
Guex, N., Peitsch, MC i Schwede, T. Zautomatyzowane modelowanie porównawcze struktury białek za pomocą SWISS-MODEL i Swiss-PdbViewer: perspektywa historyczna. Elektroforeza 30 , S162–S173 (2009).
- 37.
Bourne, Y., Taylor, P. i Marchot, hamowanie P. acetylocholinesterazy przez fascykulinę: struktura krystaliczna kompleksu. Celi 83 , 503-512 (1995).
- 38.
Bodian, DL, Davis, SJ, Morgan, BP i Rushmere, NK Analiza mutacji miejsca aktywnego i epitopów przeciwciała glikoproteiny hamującej dopełniacz, CD59. Dziennik medycyny eksperymentalnej 185 , 507-516 (1997).
- 39.
Kieffer, B. i in . Trójwymiarowa struktura roztworu pozakomórkowego regionu regulatorowego białka dopełniacza CD59, nowej domeny białkowej powierzchni komórki związanej z neurotoksynami jadu węża. Biochemia 33 , 4471-4482 (1994).
- 40.
Fletcher, CM, Harrison, RA, Lachmann, PJ & Neuhaus, D. Struktura rozpuszczalnej, glikozylowanej postaci ludzkiego białka regulatorowego dopełniacza CD59. Struktura 2 , 185-199 (1994).
- 41.
Adler, J. & Parmryd, I. Ilościowe określenie kolokalizacji przez korelację: współczynnik korelacji Pearsona jest wyższy od współczynnika nakładania się Mandera. Cytometria Część A 77 , 733-742 (2010).
- 42.
Belova, NA i Acosta-Avalos, D. Wpływ przemiennego pola magnetycznego o bardzo niskiej częstotliwości na zachowanie zwierząt w obecności pola geomagnetycznego. J Biophys 2015 , 423838 (2015).
- 43.
Wiltschko, W. & Wiltschko, R. Orientacja magnetyczna i magnetorecepcja u ptaków i innych zwierząt. J Comp Physiol A Neuroethol Sens Neural Behav Physiol 191 , 675-693 (2005).
- 44.
Lohmann, KJ Pytania i odpowiedzi: Zachowanie zwierząt: percepcja pola magnetycznego. Natura 464 , 1140-1142 (2010).
- 45.
Finn, RD i in . Pfam: baza danych rodzin białek. Badania kwasów nukleinowych 42 , D222–230.
- 46.
Isom, LL i in . Struktura pierwotna i ekspresja funkcjonalna podjednostki beta 1 kanału sodowego mózgu szczura. Science (Nowy Jork, NY) 256 , 839-842 (1992).
- 47.
Isom, LL i in . Budowa i funkcja podjednostki ²2 mózgowych kanałów sodowych, glikoproteiny przezbłonowej z motywem CAM. Celi 83 , 433-442 (1995).
- 48.
McCormick, KA i in . Molekularne determinanty funkcji kanału Na+ w domenie zewnątrzkomórkowej podjednostki beta1. Dziennik chemii biologicznej 273 , 3954-3962 (1998).
- 49.
McCormick, KA, Srinivasan, J., White, K., Scheuer, T. & Catterall, WA Domena zewnątrzkomórkowa podjednostki beta1 jest zarówno niezbędna, jak i wystarczająca do modulacji podobnej do beta1 bramkowania kanału sodowego. Dziennik chemii biologicznej 274 , 32638-32646 (1999).
- 50.
Kołomytkin, OV i in . Glikoproteiny związane z kanałami jonowymi pośredniczą w wykrywaniu pól elektrycznych: proponowany mechanizm i dowody potwierdzające. Bioelektromagnetyka 28 , 379-385 (2007).
- 51.
Lill, R. i Mühlenhoff, U. Biogeneza żelaza i siarki u eukariontów. Trendy w naukach biochemicznych 30 , 133-141 (2005).
- 52.
Malvankar, NS i in . Przestrajalne przewodnictwo metaliczne w mikrobiologicznych sieciach nanoprzewodów. Nat Nanotechnol 6 , 573-579 (2011).
- 53.
Malvankar, NS & Lovley, DR Mikrobiologiczne nanodruty do zastosowań bioenergetycznych. Curr Opin Biotechnol 27 , 88-95 (2014).
- 54.
Anderson, MA, Xu, Y. & Grissom, CB Kataliza spinów elektronowych za pomocą ksenonu w enzymie. J Am Chem Soc 123 , 6720-6721 (2001).
- 55.
Qin, S. i in . Magnetyczny biokompas białkowy. Nat Mater 15 , 217-226 (2016).
- 56.
Meister, M. Fizyczne granice magnetogenetyki. Życie 5 (2016).
- 57.
Nakajima, K. i in . KCNJ15/Kir4.2 łączy się z poliaminami, aby wykryć słabe zewnątrzkomórkowe pola elektryczne w galwanotaksji. Nat Commun 6 , 8532 (2015).
- 58.
Bellono, NW, Leitch, DB & Julius, D. Molekularne podstawy elektrorecepcji kręgowców przodków. Natura 543 , 391–396 (2017).
- 59.
Gilchrist, J., Das, S., Van Petegem, F. & Bosmans, F. Krystalograficzne wglądy w modulację kanału sodowego przez podjednostkę beta4. Proc Natl Acad Sci USA 110 , E5016-5024 (2013).
- 60.
Hoffman, GE, Le, WW & Sita, LV Znaczenie miareczkowania przeciwciał w metodach immunocytochemicznych. Curr Protoc Neurosci Rozdział 2, Część 2 12 (2008).
Podziękowanie
Autorzy dziękują dr. Frankowi Bosmansowi za uprzejme dostarczenie oocytów X. laevis oraz Megan Pino za pomoc techniczną. Praca ta była wspierana przez NIH/NINDS R01NS079288, R01NS072171, R01NS098231 i MSCRFII-0042.
Deklaracje etyczne
Konkurujące interesy
Autorzy deklarują brak sprzecznych interesów.
Dodatkowe informacje
Uwaga wydawcy: Springer Nature pozostaje neutralny w odniesieniu do roszczeń jurysdykcyjnych w opublikowanych mapach i powiązaniach instytucjonalnych.
Elektroniczny materiał uzupełniający
Film S1 A
Film S1 B
Dodatkowa informacja
Prawa i uprawnienia
Otwarty dostęp Ten artykuł jest objęty licencją Creative Commons Attribution 4.0 International License, która zezwala na używanie, udostępnianie, adaptację, dystrybucję i powielanie na dowolnym nośniku lub formacie, pod warunkiem, że przypiszesz odpowiednie uznanie oryginalnemu autorowi (autorom) i źródłu, podać link do licencji Creative Commons i wskazać, czy dokonano zmian. Obrazy lub inne materiały stron trzecich w tym artykule są objęte licencją Creative Commons tego artykułu, chyba że zaznaczono inaczej w limicie kredytowym do materiału. Jeśli materiał nie jest objęty licencją Creative Commons artykułu, a Twoje zamierzone użycie nie jest dozwolone przez przepisy ustawowe lub przekracza dozwolone użycie, musisz uzyskać pozwolenie bezpośrednio od właściciela praw autorskich. Aby wyświetlić kopię tej licencji, odwiedźhttp://creativecommons.org/licenses/by/4.0/ .
Przedruki i uprawnienia
https://www.nature.com/articles/s41598-018-27087-9







