Kristina Armitage/Quanta Magazine
Introduction

You’re the earliest known life form. There’s no food around right now. It would be great to go somewhere else. But you’re stuck. Really stuck. At your size (a couple of microns), water feels like tar, or rather, it feels the way being stuck in tar will eventually feel to a human. What do you do?
[One or more billion years later.] You’ve found the perfect solution.
Literally perfect.
“You can assume the system is working optimally,” said Aravinthan Samuel (opens a new tab), a biophysicist at Harvard University.
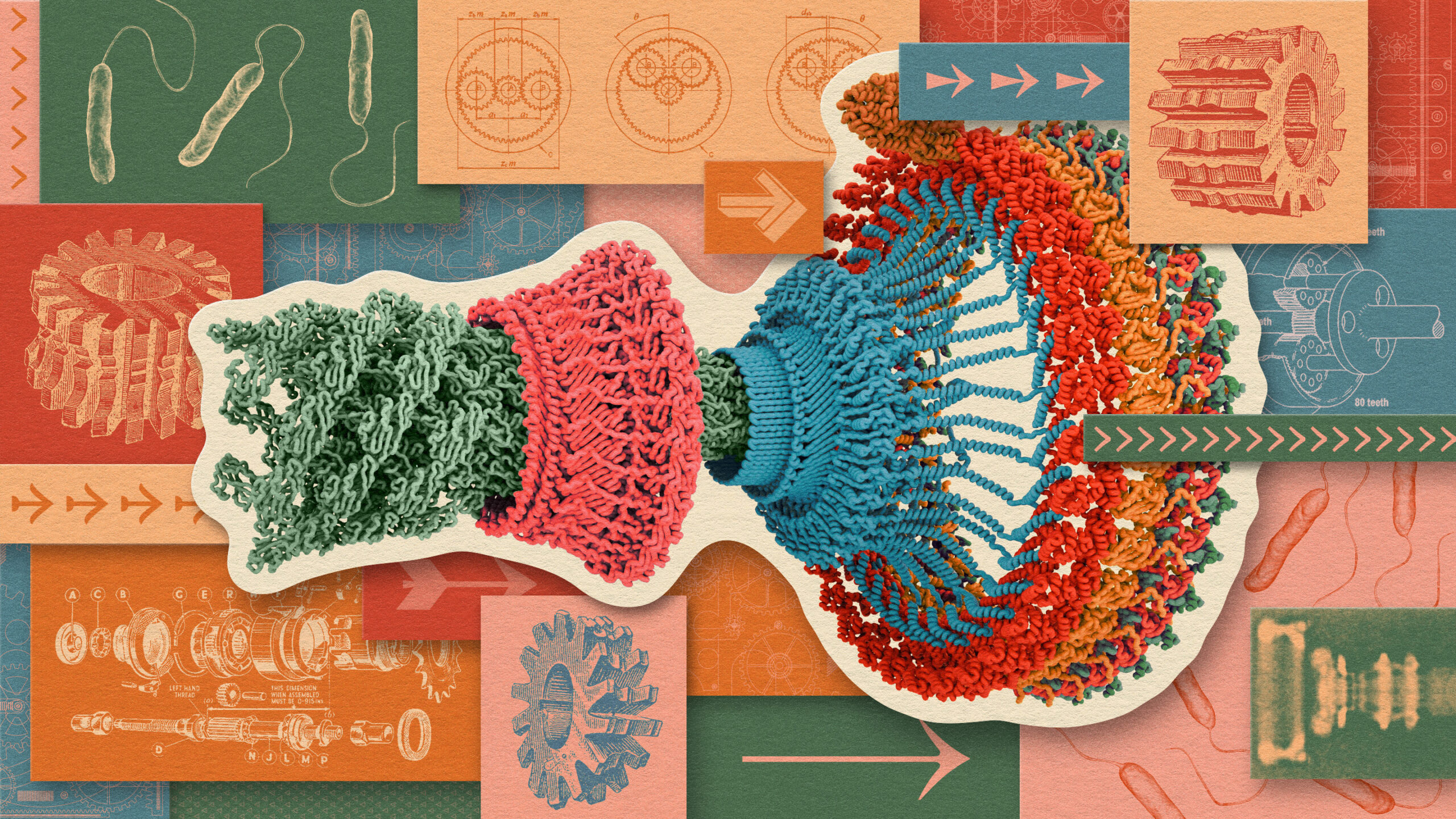
Evolution has created the flagellar motor, a combination propeller/brain that enables single-celled bacteria to move toward food sources. It’s an electric motor that rotates at several hundred revolutions per second — faster than the flywheel in a race car engine — to twirl a tail-like flagellum that pushes the cell along. When the flagellar motor rotates counterclockwise, it propels the cell through the water 10 or more times its own length in a second. The motor can also rotate clockwise, causing the cell to tumble about randomly. This amazing, self-assembling, signal-processing, direction-switching molecular machine is so powerful yet so spare that, billions of years later, it’s still used by bacteria in virtually every gut and puddle on Earth.
Since the discovery of the bacterial flagellar motor in the 1970s, biologists and creationists alike have marveled at its design like medieval architects staring with awe at the dome of the Pantheon built by their Roman ancestors. It’s hard to fathom the level of engineering achievable by a billion years of bacterial evolution, especially with only 20 minutes between cell generations, which allows for a truly astronomical number of mutations and trial runs. Creationists hold up the bacterial flagellar motor as a prime example of intelligent design — specifically the concept of “irreducible complexity,” a biological system so intricate, they say, that it couldn’t possibly have arisen in stages through the gradual, stepwise process of Darwinian evolution.
Yet it very much did. (opens a new tab)
Over the past few decades, scientists have toiled to unravel how the flagellar motor works — namely, how it rotates and switches directions.
Now they finally have. A wave of studies since 2020 has cracked the molecular structures of the flagellar motor’s parts, including, most importantly, the small cogwheels that turn the larger cogwheel at the flagellum’s base. The final pieces of this dynamic puzzle fell into place as recently as March 2026.
“My lifelong quest is now fulfilled,” said Mike Manson (opens a new tab), a professor emeritus of biophysics at Texas A&M University who started studying the flagellar motor in the 1970s. “I finally understand how this thing I’ve been studying for 50 years actually works. That’s about as satisfying as can be.”
The workings of the flagellar motor are ingenious indeed. But when I began interviewing these scientists about what they’ve figured out, I didn’t anticipate that the explanation of the motor would clarify all of biology for someone like me, who seeks mechanistic, physical explanations. The machine, I learned, exploits a driving force I had not known about (though biophysicists have) — the physical “life force” that powers processes in cells. This “proton motive force” doesn’t just turn the cogs of the flagellar motor; it’s the juice we all run on.
![]()
The flagellar motor was discovered by the late Howard Berg, an ingenious experimenter who spent most of his career at Harvard. Berg set out in the early 1970s to apply his training in physics to understanding how bacteria move. The problem was that, under a microscope, Escherichia coli, Salmonella, and other motile bacteria almost instantly swam out of frame. So Berg invented and built an automatic tracking microscope that could keep a bacterium in view as it moved around. “What it recorded were all the corrections that had to be made to the microscope stage in order to keep the bacterium in place, and that of course gives you a readout of what the path of the swimming bacterium was,” said Manson, who joined Berg’s project as a postdoc in 1975.
The data revealed that bacteria “run and tumble” — that is, they switch back and forth between swimming straight and rolling around chaotically. Berg theorized that bacteria change their swimming state based on the chemical gradients sensed as they swim. Their default behavior is to swim straight. If the concentration of sugars and other nutrients is increasing, the cell keeps going forward. If the concentration drops, it tumbles; reoriented in a new direction, the bacterium then resumes swimming straight. This process keeps the bacterium in the vicinity of harvestable molecules, which it absorbs through channels in its cell wall and membrane.
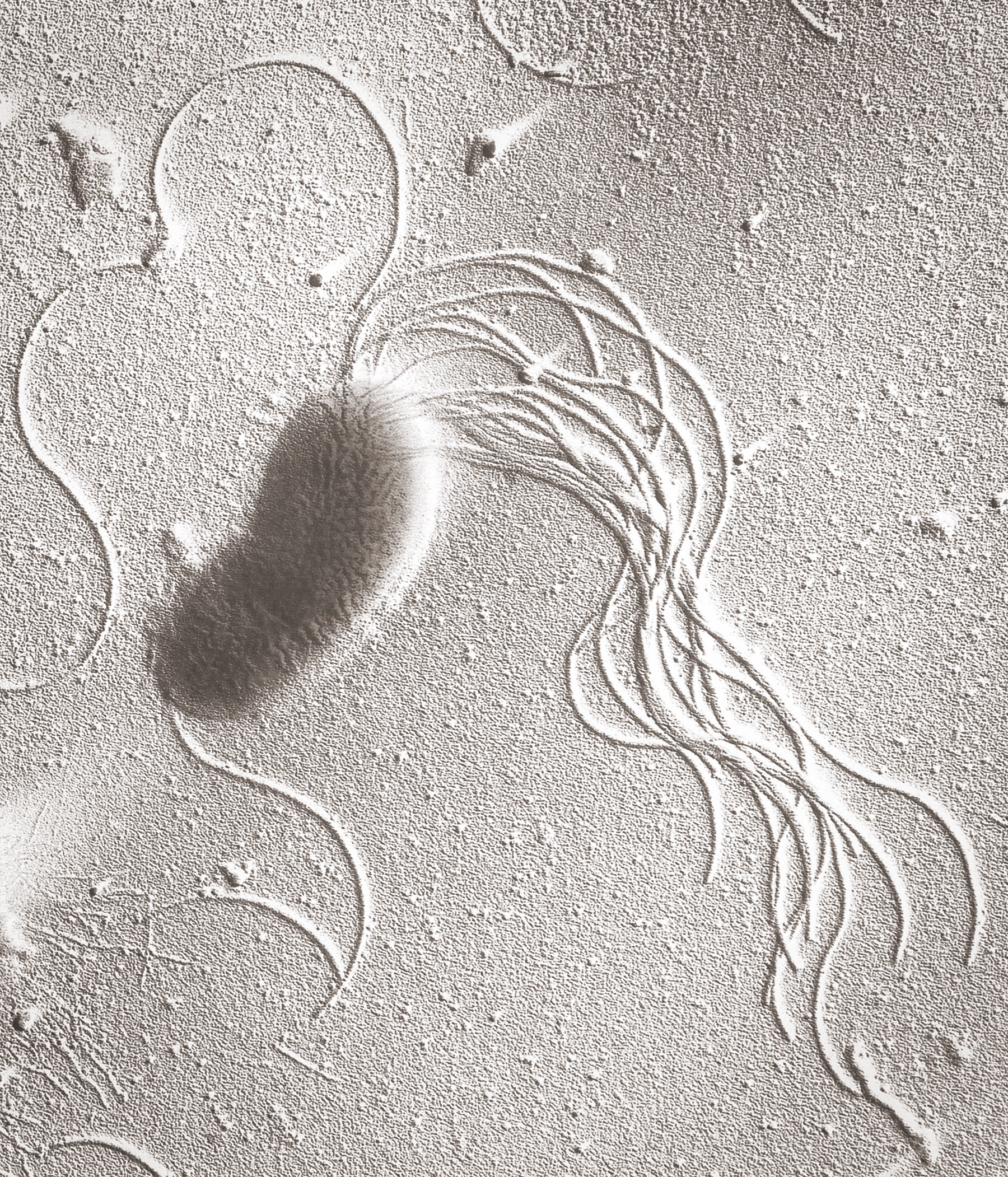
A transmission electron microscopy image reveals the cluster of flagella that a Pseudomonas fluorescens bacteria uses to move around water in soil.
Dr Tony Brain/Science Photo Library
Berg guessed that the flagellar motor was a rotor that turned the flagellum like a screw. “He did it by sticking two cells together by their flagella and seeing them spinning in opposite directions from each other,” Manson said. “From that, with no knowledge, he hypothesized that the bacterial flagellum rotates. Way ahead of his time. That was 50 years before understanding how this motor works.”
Further experiments indicated that the flagellar motor also switches direction. When its flagella — bacteria typically have several protruding from their surfaces — are all spinning counterclockwise, they form a bundle that trails behind the swimming cell like a braid in the wind, steering it straight. But as soon as one flagellar motor reverses direction and starts rotating clockwise, the bundle falls apart; the reverse-twirling filament unravels the braid and puts the cell’s flagellar motors at cross-purposes, kicking the cell around.
Before Berg’s work, “the idea of a molecular motor was bonkers — no way anything rotates,” said Samuel, Berg’s former student who now runs a Harvard lab of his own. It could wiggle, sure, but rotate? “It requires a certain geometry that people didn’t think was accessible to biology.”
Au contraire. “Biology can build wheels,” Samuel said. “Now we know.”
![]()
Improvements over the last 15 years in an imaging technique called cryo-EM (cryogenic electron microscopy) have enabled researchers to see the flagellar motor’s component parts. That has clarified how it works.
At the base of the motor is the “C ring” (or “cytoplasmic ring”), a ring of 34 identical proteins floating in the cytoplasm within the cell membrane. Scientists in the 1980s and ’90s figured out that when the C ring rotates, the flagellum does too. But why and how it rotates wasn’t obvious.
David S. Goodsell/PDB101.rcsb.ord/Modified by Quanta Magazine
The stars of the show, recent research showed, are the motor’s “stators,” smaller protein complexes that anchor themselves to the cell wall (an inner membrane) above and outside the C ring. The number of stators varies by bacterial species (E. coli has 10 or 12 available per flagellum), and how many lock into the C ring at a given time depends on the weight of the cell or the viscosity of the surrounding fluid.
Each stator consists of two central proteins that dangle from the cell wall and five proteins of a different kind that form a pentagonal ring around the pair. This pentagonal structure is the part that rubs up against the C ring.
The 5:2 geometry of the stators was revealed in 2020 (opens a new tab) in a pair of cryo-EM studies (opens a new tab), one by Susan Lea (opens a new tab) and a team at the University of Oxford, and one from a group led by Nicholas Taylor (opens a new tab) of the University of Copenhagen and Marc Erhardt (opens a new tab) of Humboldt University of Berlin. The finding pointed to a hypothesis about how the whole motor works: The stators’ pentagonal rings rotate, which then turns the larger C ring, and with it the whole flagellum.
Each pentagonal ring turns like a turnstile, one-tenth of a revolution at a time. What pushes through the turnstile is a stream of protons — the same positively charged particles found in atoms. Protons flow into cells of their own accord, for reasons I’ll get to. This is the proton motive force.
The asymmetric positioning of two proteins inside a pentagonal ring allows a proton from outside the cell to weakly bond to one of them. As the proteins jostle, the proton unbinds, exerting torque on the ring as it goes. That creates an opportunity for the same process to take place with the other central protein. In this way, protons effectively pedal the engine of the flagellar motor. Every second, more than 2,000 of them pass through the pentagonal turnstiles. In December 2025, Samuel published the results of an experiment (opens a new tab) that verified this.
Protons always want to flow into cells, never out. In passing that way, they always push the pentagonal rings clockwise. Normally, this turns the C ring counterclockwise (like the opposite turning of interlocking gears), which propels the swimming cell forward. How, though, can the flagellar motor switch directions? In 2024, another pair (opens a new tab) of cryo-EM studies (opens a new tab), from Lea, then with a team at the National Institutes of Health, and a group led by Tina Iverson (opens a new tab) at Vanderbilt University, revealed the answer.
Recall that a flagellar motor switches directions, causing the bacterium to tumble, when environmental conditions seem to be getting worse. When fewer nutritious molecules drift in, the bacterium “phosphorylates” proteins called CheY, tagging them with phosphorus atoms. Within milliseconds, phosphorylated CheY molecules diffuse around the cell, and one of them binds to one of the C-ring proteins. This small change triggers a transformation: The protein flips into a different structural configuration, which flips the next protein, and then the next. Almost instantly the whole C ring reshapes itself, like a hair clip snapping into the other of its two stable forms. Samuel’s team confirmed that the system is sensitive to a single signaling molecule (opens a new tab) in a study published in March 2026.
While the C ring is in its altered shape, the stators — the little clockwise-revolving motors — rotate against the inner edge of the C ring, rather than its outer edge. As a result, the C ring turns clockwise too. The flagellar bundle falls apart, and the cell tumbles.
Soon enough, the unstable phosphorus atom falls off the CheY protein, causing the proteins of the C ring to flip back to their original stable formation and turn counterclockwise again. The bacterium returns to forward movement, in a new direction, is search of more food.
“It’s a really elegant way of turning a unidirectional power into bidirectional rotation of the large object,” said Lea, who is now at St. Jude Children’s Research Hospital.
![]()
The proton motive force that drives the flagellar motor was proposed in 1961 by Peter Mitchell, a biochemist who worked out of his own private lab at a country estate in Cornwall, England. Though initially dismissed and even ridiculed, Mitchell went on to win the 1978 Nobel Prize in Chemistry (opens a new tab) for his idea that a current of protons constantly flows into the cell as the cell vigorously pumps them back out, and that this is the driving force behind key cellular processes.
Protons flow in because they’re diffusing from an area of high concentration (outside the cell) to an area of low concentration (inside). There are fewer than 100 free protons inside a bacterium at a time, while a similar volume of the surrounding water has tens of thousands. The cell maintains this state with machines called electron transport chains that pump out thousands of protons per second. As protons are pumped out, thousands more flow in, drawn by the net negative electric charge and the general tendency for entropy to rise as particles (in this case, protons) spread out in space ever more evenly. Cells have rigged up all kinds of molecular machines that, like water mills on rivers, take advantage of proton currents coming into the cell.
“It boggles the normal human understanding of how things work,” Manson said. “How can you have thousands and thousands of protons coming into the cell every second and still have only a few dozen inside the cell? Because they bind to something, they get pumped out again. The equilibria are so incredibly fast.”
So what makes the cell go, what breathes life into the atomic arrangements, is the efficient removal of protons so that more protons will flow. “If you were to open up a channel to protons, they would come pouring into the cell, and the proton motive force would be gone instantly,” Manson said. He’s seen this happen, when cells starve and can’t pump enough protons out. The voltage drops to nothing, and the cell’s machinery shuts down. If you’re a bacterium, your flagellar motor stops. You’re stuck.
Rarely have I loved biology more than when marveling at the flagellar motor and the influx of protons that turns its gears. “The entropic energy of the proton motive force gets converted into the kinetic energy of the rotation,” Manson said. “That’s all it is. All of it is just that. If you understand that, you basically understand the underpinnings of all that happens in biology.”
+

Kristina Armitage/ Quanta Magazine
Wstęp

Jesteś najwcześniejszą znaną formą życia. W tej chwili nie ma tu pożywienia. Wspaniale byłoby przenieść się gdzie indziej. Ale utknąłeś. Naprawdę utknąłeś. Przy twoim rozmiarze (kilka mikronów) woda przypomina smołę, a raczej przypomina to, jak człowiek będzie się czuł, będąc uwięzionym w smole. Co robisz?
[Miliard lub więcej lat później.] Znalazłeś idealne rozwiązanie.
Dosłownie idealne.
„Można założyć, że system działa optymalnie” – powiedział Aravinthan Samuel (otwiera nową kartę) , biofizyk z Uniwersytetu Harvarda.
Ewolucja stworzyła silnik wiciowy, połączenie śmigła i mózgu, które umożliwia jednokomórkowym bakteriom przemieszczanie się w kierunku źródeł pożywienia. To silnik elektryczny, który obraca się z prędkością kilkuset obrotów na sekundę – szybciej niż koło zamachowe w silniku samochodu wyścigowego – aby wirować wici przypominające ogon, która popycha komórkę. Gdy silnik wiciowy obraca się przeciwnie do ruchu wskazówek zegara, napędza komórkę w wodzie na odległość 10 lub więcej razy większą niż jej własna długość w ciągu sekundy. Silnik może również obracać się zgodnie z ruchem wskazówek zegara, powodując losowe obracanie się komórki. Ta niesamowita, samoorganizująca się, przetwarzająca sygnały i zmieniająca kierunek maszyna molekularna jest tak potężna, a jednocześnie tak oszczędna, że miliardy lat później nadal jest używana przez bakterie w praktycznie każdym jelicie i kałuży na Ziemi.
Od czasu odkrycia bakteryjnego silnika wiciowego w latach 70. XX wieku, biolodzy i kreacjoniści podziwiali jego konstrukcję niczym średniowieczni architekci wpatrujący się z podziwem w kopułę Panteonu zbudowaną przez ich rzymskich przodków. Trudno pojąć poziom inżynierii, jaki można osiągnąć dzięki miliardowi lat ewolucji bakterii, zwłaszcza przy zaledwie 20 minutach między pokoleniami komórek, co pozwala na prawdziwie astronomiczną liczbę mutacji i prób. Kreacjoniści uważają bakteryjny silnik wiciowy za doskonały przykład inteligentnego projektu – a konkretnie koncepcję „nieredukowalnej złożoności”, systemu biologicznego tak złożonego, jak twierdzą, że nie mógł on powstać etapami w stopniowym, stopniowym procesie ewolucji darwinowskiej.
A jednak tak się stało. (otwiera nową kartę)
Przez ostatnie dziesięciolecia naukowcy pracowali nad zrozumieniem, w jaki sposób działa silnik wiciowy, a konkretnie, w jaki sposób się obraca i zmienia kierunki.
W końcu im się udało. Fala badań od 2020 roku pozwoliła na rozszyfrowanie struktur molekularnych części silnika wici, w tym, co najważniejsze, małych kół zębatych, które obracają większe koło zębate u podstawy wici. Ostatnie elementy tej dynamicznej układanki znalazły się na swoim miejscu dopiero w marcu 2026 roku.
„Moje życiowe dążenie właśnie dobiegło końca” – powiedział Mike Manson (otwiera nową kartę) , emerytowany profesor biofizyki na Uniwersytecie Texas A&M, który rozpoczął badania nad silnikiem wiciowym w latach 70. XX wieku. „W końcu zrozumiałem, jak działa to, nad czym pracuję od 50 lat. To chyba najbardziej satysfakcjonujące, co może być”.
Działanie silnika wici jest rzeczywiście pomysłowe. Ale kiedy zacząłem rozmawiać z tymi naukowcami o ich odkryciach, nie spodziewałem się, że wyjaśnienie działania silnika rozjaśni całą biologię komuś takiemu jak ja, kto poszukuje mechanistycznych, fizycznych wyjaśnień. Dowiedziałem się, że maszyna wykorzystuje siłę napędową, o której nie wiedziałem (choć biofizycy wiedzieli) – fizyczną „siłę życiową”, która napędza procesy zachodzące w komórkach. Ta „siła protonowa” nie tylko wprawia w ruch tryby silnika wici; to energia, która napędza nas wszystkich.
![]()
Silnik wici został odkryty przez nieżyjącego już Howarda Berga, pomysłowego eksperymentatora, który spędził większość swojej kariery na Harvardzie. Berg postanowił na początku lat 70. wykorzystać swoją wiedzę z fizyki do zrozumienia, jak poruszają się bakterie. Problem polegał na tym, że pod mikroskopem Escherichia coli , Salmonella i inne ruchliwe bakterie niemal natychmiast wypływały poza kadr. Berg wynalazł więc i zbudował automatyczny mikroskop śledzący, który mógł utrzymywać bakterię w polu widzenia podczas jej ruchu. „Rejestrował on wszystkie poprawki, które należało wprowadzić do etapu mikroskopu, aby utrzymać bakterię na miejscu, i oczywiście dawał odczyt tego, jaka była ścieżka pływającej bakterii” — powiedział Manson, który dołączył do projektu Berga jako postdoktorant w 1975 roku.
Dane ujawniły, że bakterie „biegają i wirują” – to znaczy, naprzemiennie płyną prosto i chaotycznie. Berg wysunął teorię, że bakterie zmieniają swój sposób pływania w oparciu o gradienty chemiczne wykrywane podczas pływania. Ich domyślnym zachowaniem jest pływanie prosto. Jeśli stężenie cukrów i innych składników odżywczych rośnie, komórka kontynuuje ruch do przodu. Jeśli stężenie spada, komórka wiruje; po zmianie kierunku ruchu bakteria wraca do płynięcia prosto. Ten proces utrzymuje bakterię w pobliżu cząsteczek, które można zebrać, a które absorbuje ona kanałami w ścianie komórkowej i błonie komórkowej.

Obraz uzyskany za pomocą mikroskopu elektronowego transmisyjnego ujawnia skupisko wici, których bakteria Pseudomonas fluorescens używa do przemieszczania się wody w glebie.
Biblioteka zdjęć Dr. Tony'ego Braina/Science
Berg domyślił się, że motorem wici jest wirnik, który obraca wici niczym śrubę. „Dokonał tego, łącząc dwie komórki za wici i obserwując, jak obracają się w przeciwnych kierunkach” – powiedział Manson. „Na tej podstawie, nie mając o tym pojęcia, wysunął hipotezę, że wić bakteryjna się obraca. Znacznie wyprzedził swoją epokę. To było 50 lat przed zrozumieniem, jak działa ten motor”.
Dalsze eksperymenty wykazały, że silnik wici również zmienia kierunek. Kiedy wszystkie wici – bakterie zazwyczaj mają kilka wystających z powierzchni – obracają się przeciwnie do ruchu wskazówek zegara, tworzą wiązkę, która ciągnie się za komórką pływającą niczym warkocz na wietrze, kierując ją prosto. Jednak gdy tylko jeden z silników wici zmienia kierunek i zaczyna obracać się zgodnie z ruchem wskazówek zegara, wiązka rozpada się; wirujący w przeciwnym kierunku nić rozplata warkocz i powoduje, że silniki wici komórki działają naprzemiennie, powodując jej kołysanie.
Przed pracami Berga „idea silnika molekularnego była szalona – nie ma mowy, żeby cokolwiek się obracało” – powiedział Samuel, były student Berga, który obecnie prowadzi własne laboratorium na Harvardzie. Mógł się poruszać, owszem, ale obracać? „Wymaga to pewnej geometrii, która – jak uważano – była niedostępna dla biologii”.
Wręcz przeciwnie. „Biologia potrafi budować koła” – powiedział Samuel. „Teraz już wiemy”.
![]()
Udoskonalenia techniki obrazowania zwanej kriomikroskopią elektronową (kriogeniczna mikroskopia elektronowa) w ciągu ostatnich 15 lat umożliwiły naukowcom zobaczenie elementów składowych silnika wiciowego. To wyjaśniło, jak on działa.
U podstawy silnika znajduje się „pierścień C” (lub „pierścień cytoplazmatyczny”), pierścień 34 identycznych białek unoszących się w cytoplazmie błony komórkowej. Naukowcy w latach 80. i 90. XX wieku odkryli, że wraz z obrotem pierścienia C wici również się obracają. Jednak przyczyna i sposób obrotu nie były oczywiste.
David S. Goodsell/PDB101.rcsb.ord/Modyfikowane przez Quanta Magazine
Gwiazdami spektaklu, jak wykazały najnowsze badania, są „statory” silnika, mniejsze kompleksy białkowe, które zakotwiczają się w ścianie komórkowej (błonie wewnętrznej) powyżej i na zewnątrz pierścienia C. Liczba statorów różni się w zależności od gatunku bakterii ( E. coli ma ich 10 lub 12 na wici), a liczba, która w danym momencie blokuje się w pierścieniu C, zależy od masy komórki lub lepkości otaczającego płynu.
Każdy stator składa się z dwóch centralnych białek, które zwisają ze ściany komórkowej, oraz pięciu białek różnego rodzaju, które tworzą pięciokątny pierścień wokół pary. Ta pięciokątna struktura to część, która ociera się o pierścień C.
Geometria stojanów 5:2 została ujawniona w 2020 roku (otwiera nową kartę) w dwóch badaniach kriomikroskopii elektronowej (otwiera nową kartę) , jednym przeprowadzonym przez Susan Lea (otwiera nową kartę) i zespół z Uniwersytetu Oksfordzkiego, a drugim przez grupę kierowaną przez Nicholasa Taylora (otwiera nową kartę) z Uniwersytetu Kopenhaskiego i Marca Erhardta (otwiera nową kartę) z Uniwersytetu Humboldta w Berlinie. Odkrycie to wskazało na hipotezę dotyczącą działania całego silnika: pięciokątne pierścienie stojanów obracają się, co powoduje obrót większego pierścienia C, a wraz z nim całej wici.
Każdy pięciokątny pierścień obraca się jak kołowrót, z prędkością jednej dziesiątej obrotu na raz. Przez kołowrót przechodzi strumień protonów – tych samych dodatnio naładowanych cząstek, które występują w atomach. Protony wpływają do komórek samoistnie, z powodów, o których opowiem. To właśnie jest siła protonowo-motoryczna.
Asymetryczne ułożenie dwóch białek wewnątrz pięciokątnego pierścienia pozwala protonowi spoza komórki na słabe wiązanie się z jednym z nich. Gdy białka się przepychają, proton odłącza się, wywierając moment obrotowy na pierścień. Stwarza to możliwość zajścia tego samego procesu z drugim białkiem centralnym. W ten sposób protony skutecznie napędzają silnik wici. Co sekundę ponad 2000 z nich przechodzi przez pięciokątne kołowroty. W grudniu 2025 roku Samuel opublikował wyniki eksperymentu (otwiera nową kartę), który to potwierdził.
Protony zawsze chcą wpływać do komórek, nigdy na zewnątrz. Przechodząc w ten sposób, zawsze popychają pierścienie pięciokątne zgodnie z ruchem wskazówek zegara. Zwykle powoduje to obrót pierścienia C w kierunku przeciwnym do ruchu wskazówek zegara (jak w przypadku zazębiających się kół zębatych), co napędza pływającą komórkę. Jak jednak silnik wici może zmieniać kierunki? W 2024 roku kolejna para (otwiera nową kartę) badań kriomikroskopowych ( otwiera nową kartę) , prowadzonych przez Lea, wówczas z zespołem z Narodowych Instytutów Zdrowia (NIH), oraz grupą kierowaną przez Tinę Iverson (otwiera nową kartę) z Uniwersytetu Vanderbilt, ujawniła odpowiedź.
Przypomnijmy, że silnik wiciowy zmienia kierunek, powodując ruch bakterii wirowej, gdy warunki środowiskowe wydają się pogarszać. Gdy napływa mniej cząsteczek odżywczych, bakteria „fosforyluje” białka zwane CheY, oznaczając je atomami fosforu. W ciągu milisekund fosforylowane cząsteczki CheY dyfundują po komórce, a jedna z nich wiąże się z jednym z białek pierścienia C. Ta niewielka zmiana uruchamia transformację: białko zmienia konfigurację strukturalną, która powoduje zmianę konfiguracji kolejnego białka, a następnie kolejnego. Niemal natychmiast cały pierścień C przekształca się, niczym spinka do włosów, która wskakuje w drugą ze swoich dwóch stabilnych form. Zespół Samuela potwierdził, że system jest wrażliwy na pojedynczą cząsteczkę sygnałową (otwiera nową kartę) w badaniu opublikowanym w marcu 2026 roku.
Podczas gdy pierścień C ma zmieniony kształt, stojany – małe silniczki obracające się zgodnie z ruchem wskazówek zegara – obracają się wokół wewnętrznej krawędzi pierścienia C, a nie wokół jego zewnętrznej krawędzi. W rezultacie pierścień C również obraca się zgodnie z ruchem wskazówek zegara. Pęczek wici rozpada się, a komórka obraca się.
Wkrótce niestabilny atom fosforu odpada od białka CheY, powodując, że białka pierścienia C powracają do swojej pierwotnej, stabilnej struktury i ponownie obracają się przeciwnie do ruchu wskazówek zegara. Bakteria powraca do ruchu do przodu, w nowym kierunku – w poszukiwaniu pożywienia.
„To naprawdę elegancki sposób na przekształcenie jednokierunkowej mocy w dwukierunkowy obrót dużego obiektu” – powiedział Lea, który obecnie pracuje w szpitalu dziecięcym St. Jude Children's Research Hospital.
![]()
Siła protonowa, która napędza silnik wici, została zaproponowana w 1961 roku przez Petera Mitchella, biochemika pracującego w swoim prywatnym laboratorium w wiejskiej posiadłości w Kornwalii w Anglii. Choć początkowo odrzucony, a nawet wyśmiany, Mitchell otrzymał w 1978 roku Nagrodę Nobla w dziedzinie chemii (otwiera nową kartę) za swoją teorię, że strumień protonów stale napływa do komórki, gdy komórka energicznie je wypompowuje, i że jest to siła napędowa kluczowych procesów komórkowych.
Protony napływają, ponieważ dyfundują z obszaru o wysokim stężeniu (na zewnątrz komórki) do obszaru o niskim stężeniu (wewnątrz). Wewnątrz bakterii znajduje się mniej niż 100 wolnych protonów na raz, podczas gdy podobna objętość otaczającej ją wody zawiera dziesiątki tysięcy. Komórka utrzymuje ten stan za pomocą maszyn zwanych łańcuchami transportu elektronów, które pompują tysiące protonów na sekundę. W miarę jak protony są pompowane, tysiące kolejnych napływają, przyciągane przez wypadkowy ujemny ładunek elektryczny i ogólną tendencję wzrostu entropii, ponieważ cząstki (w tym przypadku protony) rozprzestrzeniają się w przestrzeni coraz bardziej równomiernie. Komórki wyposażyły się w różnego rodzaju maszyny molekularne, które, niczym młyny wodne na rzekach, wykorzystują prądy protonów napływające do komórki.
„To zadziwiające dla normalnego ludzkiego rozumienia, jak to wszystko działa” – powiedział Manson. „Jak to możliwe, że tysiące protonów dociera do komórki co sekundę, a w środku pozostaje tylko kilkadziesiąt? Ponieważ wiążą się z czymś, są ponownie wydalane. Równowagi zachodzą niewiarygodnie szybko”.
Zatem tym, co napędza komórkę, co tchnie życie w układy atomowe, jest efektywne usuwanie protonów, aby umożliwić przepływ większej ich liczby. „Gdybyśmy otworzyli kanał dla protonów, wlałyby się one do komórki, a siła napędowa protonów natychmiast by zniknęła” – powiedział Manson. Widział to, gdy komórki głodują i nie są w stanie wypompować wystarczającej ilości protonów. Napięcie spada do zera, a mechanizm komórkowy przestaje działać. Jeśli jesteś bakterią, twój silnik wiciowy przestaje działać. Jesteś w impasie.
Rzadko kiedy kochałem biologię bardziej niż wtedy, gdy podziwiałem silnik wiciowy i napływ protonów, który wprawia go w ruch. „Entropijna energia siły protonowej przekształca się w energię kinetyczną obrotu” – powiedział Manson. „To wszystko. To po prostu to. Jeśli to zrozumiesz, zrozumiesz podstawy wszystkiego, co dzieje się w biologii”.

+
https://www.quantamagazine.org/what-physical-life-force-turns-biologys-wheels-20260420/







